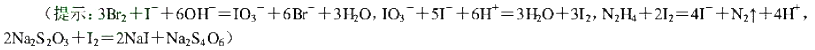题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
少量的碘化物可利用“化学放大”反应进行测定,其步骤如下:在中性或弱酸性介质中先加Br2</sub>然后
少量的碘化物可利用“化学放大”反应进行测定,其步骤如下:在中性或弱酸性介质中先加Br2然后加入过量的KI,用CCL4萃取生成的I2(萃取率E=100% )。分去水相后,用肼(即联氨)的水溶液将I2反萃至水相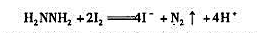 ,再用过量的Br2氧化,除去剩余的Br2后加入过量KI,酸化,以淀粉作指示剂,用Na2S2O3标准溶液滴定,求得I2的含量。
,再用过量的Br2氧化,除去剩余的Br2后加入过量KI,酸化,以淀粉作指示剂,用Na2S2O3标准溶液滴定,求得I2的含量。
a.写出上述过程的有关反应方程式;
b.根据有关的反应计量关系,说明经上述步骤后,试样中1mol的I可消耗几摩尔Na2S2O3相当于“放大”到多少倍?
c.若在测定时,准确移取含KI的试液25.00mL。终点时耗用0.100mol·1L-1Na2S2O3溶液20.06mL,试计算试液中KI的浓度(g.L-1)。已知MKI=166g·mol-1
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)

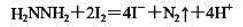 。
。