 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
同一温度和压力下,一定量某物质的熵值是()。
A.S(气)<S(液)<S(固)
B.S(气)>S(液)>S(固)
C.S(液)>S(气)>S(固)
D.S(液)>S(固)>S(气)
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 B,占比21.05%
- · 有4位网友选择 B,占比21.05%
- · 有4位网友选择 A,占比21.05%
- · 有2位网友选择 D,占比10.53%
- · 有2位网友选择 A,占比10.53%
- · 有2位网友选择 D,占比10.53%
- · 有1位网友选择 C,占比5.26%



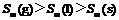
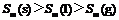
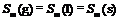
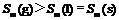
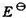 =0.9265V;
=0.9265V;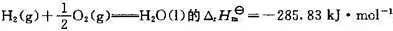 ;
;
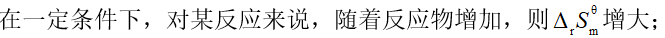
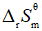 增大;
增大;




























