 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


某一元弱碱的共轭酸的水溶液浓度为0.1mol/L,其PH值为3.48,该弱碱的PKb的近似值应为10.04。此题为判断题(对,错)。
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有5位网友选择 对,占比62.5%
- · 有3位网友选择 错,占比37.5%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“某一元弱碱的共轭酸的水溶液浓度为0.1mol/L,其PH值为3.48,该弱碱的PKb的近似值应为10.04。”相关的问题
更多“某一元弱碱的共轭酸的水溶液浓度为0.1mol/L,其PH值为3.48,该弱碱的PKb的近似值应为10.04。”相关的问题
已知0.10mol.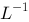 一元弱碱
一元弱碱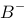 的pH = 8.0,則其0.10mol.
的pH = 8.0,則其0.10mol.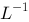 的共轭酸HB溶液的pH 是
的共轭酸HB溶液的pH 是
A、2.0
B、3.0
C、3,5
D、4,0
分析不纯CaCO3(其中不含分析干扰物)时,称取试样0.3000克,加入0.2500M HCl标准溶液25.00ml。煮沸除去CO2,用0.2012MNaOH溶液返滴过量酸,消耗了5.84ml。计算试样中CaCO3的百分含量。 1. 为什么用作滴定分析的化学反应必须有确定的计量关系?什么是“化学计量点”?什么是“终点”?为什么滴定分析对化学反应进行的完全程度的要求比重量分析高? 2. 指出下列各酸的共轭碱:HAc, H2CO3,HCO3- ,H3PO4, H2PO4-, NH4+, H2S ,HS- 3. 指出下列各碱的共轭酸:Ac-, CO32- ,PO43-,HPO42- ,S2- ,NH3 ,CN-,OH-。 4. 根据下列反应,标出共轭酸碱对。 (1) H2O+H2O H3O++OH- (2) HAc+H2O H3O+Ac- (3) H3PO4+OH- H2PO4-+H2O (4)CN-+H2O HCN+H2O 5. 指出下列物质中的共轭酸、共轭碱,并按照强弱顺序排列起来:HAc,Ac-;NH4+,NH3;HF,F-;H3PO4,H2PO4-;H2S,HS-。 6.已知下列各酸的pKa和弱碱的pKb值,求它们的共轭碱和共轭酸的pKb和pKa (1)HCN pKa=9.31 (2) NH4+ pKa=9.25 (3) HCOOH pKa=3.75 (4) 苯胺 pKb=9.34 7. 计算0.10mol•L-1甲酸(HCOOH)溶液的pH值及其离解度。 表Ka=1.77×10-4 8.取含惰性杂质的混合碱(含NaOH,NaCO3,NaHCO3或它们的混合物)试样一份,溶解后,以酚酞为指示剂,滴至终点消耗标准酸液V1ml;另取相同质量的试样一份,溶解后以甲基橙为指示剂,用相同的标准溶液滴至终点,消耗酸液V2ml,(1)如果滴定中发现2V1=V2,则试样组成如何?(2)如果试样仅含等摩尔NaOH和Na2CO3,则V1与V2有何数量关系? 9.称取含NaH2PO4和Na2HPO4及其他惰性杂质的试样1.000g,溶于适量水后,以百里酚酞作指示剂,用0.1000mol•L-1NaOH标准溶液滴至溶液刚好变蓝,消耗NaOH标准溶液20.00ml,而后加入溴甲酚绿指示剂,改用0.1000 mol•L-1HCl标准溶液滴至终点时,消耗HCl溶液30.00ml,试计算:(1)W(NaH2PO4),(2)W(Na2HPO4),(3)该NaOH标准溶液在甲醛法中对氮的滴定度。 10.何为基准物质?必须具备那些条件? 11.HCl与HAc的混合溶液(浓度均为0.10 mol•L-1),能否以甲基橙为指示剂,用0.1000 mol•L-1 NaOH溶液直接滴定其中的HCl?此变色点时有多少H Ac参与了反应? 12.一试液可能是NaOH、NaHCO3、Na2CO3或它们的固体混合物的溶液。用20.00mL 0.1000 mol•L-1HCl标准溶液,以酚酞为指示剂可滴定至终点。问在下列情况下,继以甲基橙作指示剂滴定至终点,还需加入多少毫升HCl溶液? (1)试液中所含NaOH与Na2CO3、物质的量比为3∶1; (2)原固体试样中所含NaHCO3和NaOH的物质量比为2∶1;

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
