 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友seven1982112
发布时间:2022-01-06
[主观题]
试指出一周期主族元素含氧酸的氧化性变化规律,举出实例并讨论这种规律的形成原因。同一周期副族元
素含氧酸的氧化性变化规律如何?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
查看官方参考答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“试指出一周期主族元素含氧酸的氧化性变化规律,举出实例并讨论这种规律的形成原因。同一周期副族元”相关的问题
更多“试指出一周期主族元素含氧酸的氧化性变化规律,举出实例并讨论这种规律的形成原因。同一周期副族元”相关的问题
下表是某些短周期元素的电负性(用x表示)的数值:
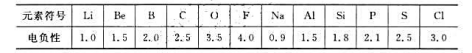
(1)通过分析上表中电负性的数值变化的规律,试确定Mg和N元素的电负性的数值范围() < x(Mg) < ()和() < x(N )< ()。
(2)同周期(同主族)元素的电负性与原子半径的关系是()。
(3)当形成化学键的两种元素的电负性的差值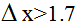 时,一般为离子键;当
时,一般为离子键;当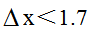 时,一般为共价键。则由此可知AlBr3中化学键的类型是()。
时,一般为共价键。则由此可知AlBr3中化学键的类型是()。
A.原子半径:丁>丙>乙>甲
B.单质的氧化性:乙>丙>丁
C.气态氢化物稳定性:乙>丙>丁
D.甲与乙、丙、丁形成的化合物均为共价化合物
A.铊是易导电的银白色金属
B.能生成+3价离子
C.氢氧化铊是两性氢氧化物
D.Tl3+的氧化性比Al3+强
A.X属于非金属元素
B.对应的氢化物的热稳定性:W>Y
C.W与Z易于形成离子化合物
D.Z离子的氧化性强于X离子
A.离子半径:X>Y>Z>W
B.Y的气态氢化物稳定性强于Z的气态氢化物稳定性
C.Z的最高价含氧酸酸性强于Y的最高价含氧酸酸性
D.Y与W两种元素形成的化合物只有一种

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
