 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某原电池反应的离子方程式为Fe+2H+=Fe2++H2↑,下列说法正确的是()
A.可用硝酸作电解质溶液
B.可用锌作原电池正极
C.用铁作负极,铁的质量不变
D.可用铜作原电池正极
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 B,占比44.44%
- · 有2位网友选择 C,占比22.22%
- · 有2位网友选择 D,占比22.22%
- · 有1位网友选择 A,占比11.11%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.可用硝酸作电解质溶液
B.可用锌作原电池正极
C.用铁作负极,铁的质量不变
D.可用铜作原电池正极
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“某原电池反应的离子方程式为Fe+2H+=Fe2++H2↑,下列说法正确的是()”相关的问题
更多“某原电池反应的离子方程式为Fe+2H+=Fe2++H2↑,下列说法正确的是()”相关的问题
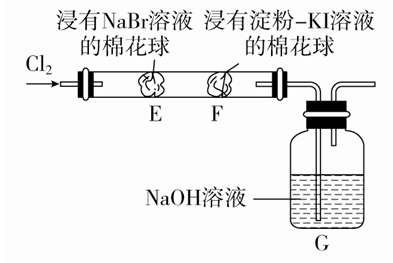
A.E处棉花球变成橙色,说明Cl的非金属性比Br强
B.F处棉花球变成蓝色,说明Br2的氧化性比I2强
C.E处发生反应的离子方程式为Cl2+2Br-===2Cl-+Br2
D.G装置中NaOH溶液与Cl2反应的离子方程式为2OH-+Cl2===ClO-+Cl-+H2O
A.反应过程中能量关系如上图表示,则该反应为放热反应
B.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L
C.化学反应的焓变与反应方程式的计量系数有关
D.若将该反应设计成原电池,锌为负极
A.反应过程中能量关系如上图表示,则该反应为放热反应
B.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L
C.化学反应的焓变与反应方程式的计量系数有关
D.若将该反应设计成原电池,锌为负极
(1)写出电池反应方程式;
(2)由附表六查得Eθ(Cl2/Cl-),计算E(Co2+/Co);
(3)p(Cl2)增大时,电池的电动势将如何变化?
(4)当CO2+浓度为0.010mol·L-1其他条件不变时,电池的电动势是多少伏?
已知: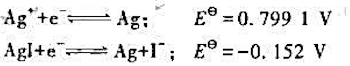 (1)写出由上列两个半反应组成的原电池符号;
(1)写出由上列两个半反应组成的原电池符号;
(2)写出电池反应方程式;
(3)求 值。
值。
在pH=2,其他有关离子浓度为1.0 mol·L-1时,将电对 ,Fe1+/Fe2+组装成原电池,计算原电池的电动势,写出电极反应、电池反应。已知
,Fe1+/Fe2+组装成原电池,计算原电池的电动势,写出电极反应、电池反应。已知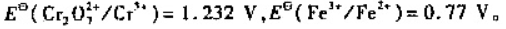

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
