 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
双原子分子中电子能E电子、平动能E平动、转动能E转动和振动能E振动的大小顺序为( )
A.E平动<E转动<E振动<E电子
B.E振动<E平动<E转动<E电子
C.E平动<E振动<E转动<E电子
D.E转动<E平动<E振动<E电子
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有3位网友选择 E,占比33.33%
- · 有3位网友选择 D,占比33.33%
- · 有2位网友选择 C,占比22.22%
- · 有1位网友选择 B,占比11.11%



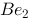 ,
,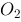 两种
两种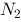 ,
,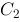 两种
两种 ,
,




























