 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有Cu2+和Ag+的混合溶液,其浓度分别是1 mol/L及0.01 mol/L, 以铂为电极进行电解,在阳极首先析出的是Ag还是Cu,电解时两种金属离子能否分开?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“有Cu2+和Ag+的混合溶液,其浓度分别是1 mol/L及0.01 mol/L, 以铂为电极进行电解,在阳极首先析出的是Ag还是Cu,电解时两种金属离子能否分开?”相关的问题
更多“有Cu2+和Ag+的混合溶液,其浓度分别是1 mol/L及0.01 mol/L, 以铂为电极进行电解,在阳极首先析出的是Ag还是Cu,电解时两种金属离子能否分开?”相关的问题
等体积混合0.30mol·L-1NH3溶液、0.30mol·L-1NaCN溶液和0.030mol·L-1AgNO3溶液,求平衡时[Ag(CN)2]-和[Ag(NH3)2]+的浓度。已知Kf([Ag(CN)2]-)=1.26×1021,Kf([Ag(NH3)2]+)=1.6×107。
电解Cu2+和Sn2+的混合酸性溶液,Cu2+和Sn2+的浓度均为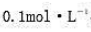 ,以铂为电极进行电解。
,以铂为电极进行电解。
(1)在阴极上何种离子先析出?
(2)若要使两种金属离子完全分开,阴极电位应控制多少?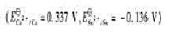
CN,求溶液中[Ag(NO2)2]-,[Ag(NO)2]-, 及CN-等各种离子的平衡浓度(忽略体积变化,已知
及CN-等各种离子的平衡浓度(忽略体积变化,已知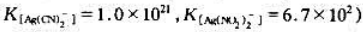 .
.
将10.0mL0.10mol·L-1AgNO3溶液与10.0mL1.0mol·L-1氨水混合,计算反应达平衡时Ag+的浓度;若以10.0mL1.0mol·L-1NaCN溶液代替氨水,平衡后溶液Ag+的浓度又是多少?已知Ks([Ag(NH3)2]+)=1.1×107,Ks([Ag(CN)2]-)=1.3×1021。
K[Ag(CN)2-]=1.0X1021,K[Ag(NH3)]2+=-1.6X107.
将Pb(NO3)2溶液与BaCl2溶液混合,设混合液中Pb(NO3)2的浓度为0.20 molL-1,同: (1)在混合溶液中Cl-的浓度等于5.0 × 10-4molL-1时,是否有沉淀生成? (2)混合溶液中Cl-的浓度多大时,开始生成沉淀? (3)混合溶液中Cl-的浓度为6.0 × 10-2molL-1时,残留于溶液中Pb2+的浓度为多少?
A.5.9×10-9
B.8.9×10-9
C.4.6×10-9
D.7.3×10-9
25℃时,以铂作电极,以1.0mol·dm-3KOH水溶液作电解质溶液,分别用纯净的压力为1.00×105Pa的氢气和氧气通于两极,组成原电池。
欲以0.020mol·dm-3EDTA溶液滴定相同浓度的Pb2+和Ca2+混合溶液中的Pb2+。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
