 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法是否正确?为什么?(1)可通过热处理来明显改善灰铸铁的力学性能;(2)可锻铸铁因具有较好的塑性,故可进行锻造;(3)白口铸铁硬度高,可用于制造刀具;(4)因片状石墨的影响,灰铸铁的各项力学性能指标均远低于钢。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“下列说法是否正确?为什么?(1)可通过热处理来明显改善灰铸铁的力学性能;(2)可锻铸铁因具有较好的塑性,故可进行锻造;(3)白口铸铁硬度高,可用于制造刀具;(4)因片状石墨的影响,灰铸铁的各项力学性能…”相关的问题
更多“下列说法是否正确?为什么?(1)可通过热处理来明显改善灰铸铁的力学性能;(2)可锻铸铁因具有较好的塑性,故可进行锻造;(3)白口铸铁硬度高,可用于制造刀具;(4)因片状石墨的影响,灰铸铁的各项力学性能…”相关的问题
下列说法是否正确?为什么?
(1)每一个幂级数在它的收敛圆周上处处收敛;
(2)每一个幂级数的和函数在收敛圆内可能有奇点;
(3)每一个在z0连续的函数一定可以在z0的邻域内展开成泰勒级数.
下列说法是否正确,为什么?
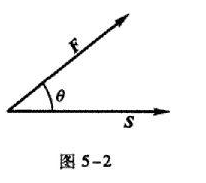
(1)与x、y、z三坐标轴的正向夹角相等的向量,其方向角为(π/3,π/3,π/3)
(2) 2i>j;
(3)如图5-2所示,则力F在向量S上的分力为Fcosθ.
A.不能,因为加水和溢流活门只有电动开关功能
B. 可以,因为加水和溢流活门可通过手柄及推拉钢索操作
C. 不能,因为断电后加水和溢流活门会被锁在关位
D. 可以,因为热电瓶汇流条会给加水和溢流活门供电
判断下列说法是否正确,为什么?
(1)如线性规划的原问题存在可行解,则其对偶问题也一定存在可行解;
(2)如线性规划的对偶问题无可行解,则原问题也一定无可行解;
(3)如果线性规划的原问题和对偶问题都具有可行解,则该线性规划问题一定具有有限最优解。
下列说法是否正确,为什么?
①主量子数为1时,有两个方向相反的轨道;
②主量子数为2时,有2s、2p两个轨道;
③主量子数为2时,有4个轨道,即2s、2p、2d、2f;
④因为H原子中只有1个电子,故它只有1个轨道;
⑤当主量子数为2时,其角量子数只能取1个数,即l=1;
⑥任何原子中,电子的能量只与主量子数有关。
对于可逆反应:
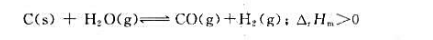
下列说法是否正确?为什么?
(1)达到化学平衡时各反应物和生成物的分压一定相等;
(2)改变生成物的分压,使
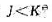 ,化学平衡向右移动;
,化学平衡向右移动;
(3)升高温度使正反应速率增大,逆反应速率减小,故化学平衡向右移动;
(4)由于反应前后分子数相等,所以增大压力对化学平衡没有影响;
(5)加入催化剂使正反应速率增大,化学平衡向右移动。
下列说法是否正确?为什么? (1)因为![下列说法是否正确?为什么? (1)因为 [图] ,所以 [图...下列说法是否正确?为什么?](http://static.jiandati.com/c1ccc74-chaoxing2016-353269.png) ,所以
,所以![下列说法是否正确?为什么? (1)因为 [图] ,所以 [图...下列说法是否正确?为什么?](http://static.jiandati.com/6fda879-chaoxing2016-353270.png) 就是标准态下的平衡常数。 (2)
就是标准态下的平衡常数。 (2)![下列说法是否正确?为什么? (1)因为 [图] ,所以 [图...下列说法是否正确?为什么?](http://static.jiandati.com/6fda879-chaoxing2016-353270.png) 的数值不但与温度、方程式的写法有关,还与标准态的选择有关。 (3)当
的数值不但与温度、方程式的写法有关,还与标准态的选择有关。 (3)当![下列说法是否正确?为什么? (1)因为 [图] ,所以 [图...下列说法是否正确?为什么?](http://static.jiandati.com/18dbe8f-chaoxing2016-353271.png) ,反应一定不能自发正向进行。 (4)对理想气体的化学反应,当温度一定时,
,反应一定不能自发正向进行。 (4)对理想气体的化学反应,当温度一定时,![下列说法是否正确?为什么? (1)因为 [图] ,所以 [图...下列说法是否正确?为什么?](http://static.jiandati.com/cb15a9f-chaoxing2016-353272.png) 有定值,因此其平衡组成不变。 (5)复相反应中,平衡常数的表达式中并没有出现凝聚相的分压成浓度项,因此,计算此类反应的
有定值,因此其平衡组成不变。 (5)复相反应中,平衡常数的表达式中并没有出现凝聚相的分压成浓度项,因此,计算此类反应的![下列说法是否正确?为什么? (1)因为 [图] ,所以 [图...下列说法是否正确?为什么?](http://static.jiandati.com/efb6f9c-chaoxing2016-353273.png) 只需考虑参与反应的气相物质。
只需考虑参与反应的气相物质。
判断下列命题(或说法)是否正确,为什么?
(1) 如果向量β可由向量组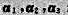 线性表示, 即
线性表示, 即 则表示系数
则表示系数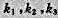 不全为零
不全为零
(2)若向量组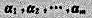 是线性相关的,则a1一定可由
是线性相关的,则a1一定可由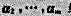 线性表示:
线性表示:
(3)若向量组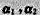 线性相关, 向量组
线性相关, 向量组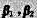 线性相关,则有不全为零的数
线性相关,则有不全为零的数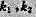 使
使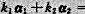 0且
0且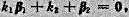 从而使
从而使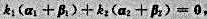 故
故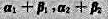 线性相关;
线性相关;
(4)如果存在不全为零的数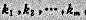 使
使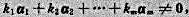 则向量组
则向量组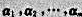 线性无关;
线性无关;
(5)若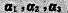 线性无关
线性无关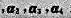 线性相关, 则a1不可由
线性相关, 则a1不可由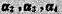 线性表示
线性表示

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
