 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
压力为80cmHg时,气体之体积为1000cm3,如温度不变,而体...
压力为80cmHg时,气体之体积为1000cm3,如温度不变,而体积增至2000cm3,问压力应为多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
压力为80cmHg时,气体之体积为1000cm3,如温度不变,而体积增至2000cm3,问压力应为多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“压力为80cmHg时,气体之体积为1000cm3,如温度不变,而体...”相关的问题
更多“压力为80cmHg时,气体之体积为1000cm3,如温度不变,而体...”相关的问题
计算1mol理想气体在下列四个过程中所作的体积功.已知始态体积为25dm3,终态体积为100dm3,始态及终态温度均为100℃.
(1)向真空膨胀;
(2)在外压力恒定为气体终态的压力下膨胀;
(3)先在外压力恒定为体积等于50dm3时的气体的平衡压力下膨胀,当膨胀到50dm3(此时温度仍为100℃)以后,再在外压力等于100dm3时气体的平衡压力下膨胀;
(4)等温可逆膨胀.试比较这四个过程的功,比较的结果说明了什么问题?
A.500
B.100
C.200
D.150
(1)将气体总压降低,直至体积为2dm3;
(2)总压保持在101.3kPa的条件下,通人N2,至体积变为2dm3;
(3)保持体积为1dm3的条件下,通入N2使压力增至202.6kPa;
(4)保持体积为1dm3的条件下,通入Cl2使压力增至202.6kPa;
(5)保持总压为101.3kPa的条件下,通入Cl2使体积增至2dm3.
A.12.3,12.3;
B.8.24,8.24;
C.12.3,8.24;
D.8.24,12.3
在等温条件下,1.00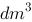 密闭容器中装有A和B的混合气体,其总压力为100 kPa,气体A的分压为50 kPa,则下列说法中不正确的是
密闭容器中装有A和B的混合气体,其总压力为100 kPa,气体A的分压为50 kPa,则下列说法中不正确的是
A、A的摩尔分数为0.50
B、A与B的物质的量相等
C、A的分体积为0.50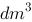
D、A与B物质的量之比为1∶2
A、B两种气体在体积为V的容器中混合,在温度T时测得混合气体的压力为P。若VA、VB分别为两种气体的分体积,PA、PB分别为两种气体的分压力,下列计算式中不正确的一个是
(A) pVA=nART (B) PAVA=nART (C) PAV=nART (D) pA(VA+VB)=nART

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
