 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在20℃、pθ下,将1mol NH3(g)溶于组成为nNH3:nH2O=1:30的大量溶液中,求此过程的△G。已知该溶液上方氨
在20℃、pθ下,将1mol NH3(g)溶于组成为nNH3:nH2O=1:30的大量溶液中,求此过程的△G。已知该溶液上方氨的平衡蒸气分压为3.60x103Pa。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在20℃、pθ下,将1mol NH3(g)溶于组成为nNH3:nH2O=1:30的大量溶液中,求此过程的△G。已知该溶液上方氨的平衡蒸气分压为3.60x103Pa。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“在20℃、pθ下,将1mol NH3(g)溶于组成为nNH3:nH2O=1:30的大量溶液中,求此过程的△G。已知该溶液上方氨”相关的问题
更多“在20℃、pθ下,将1mol NH3(g)溶于组成为nNH3:nH2O=1:30的大量溶液中,求此过程的△G。已知该溶液上方氨”相关的问题
A.标准状况下56 g 铁原子
B.20℃、101 kPa时36.5g HCl
C.标准状况下6.02×10^23个NH3
D.标准状况下1mol C2H5OH
A.1mol;
B.2mol;
C.0.5mol;
D.4mol。
A.∆U = T∆S
B.∆S = (∆H- ∆G)/T
C.∆H = T∆S + V∆p
D.∆GT,p = 0
293K时,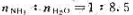 的氨水溶液(A)上NH3的蒸气压为1.07×104Pa,而
的氨水溶液(A)上NH3的蒸气压为1.07×104Pa,而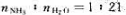 的氨水溶液(B)上NH3;的蒸气压为3.60×103Pa.计算:
的氨水溶液(B)上NH3;的蒸气压为3.60×103Pa.计算:
(1)将1.00molNH3从大量溶液A中转移到大量溶液B中的ΔG;
(2)293K下,将压力为pθ的1.00molNH3(g)溶于大量溶液B中,NH3的ΔG.
反应N3(g)+3H3(g)=2NH3(g)在一定温度下达平衡状态时,系统内n(N2)=4mol,n(H2)=n(NH3)=1mol。保持系统压力和温度恒定条件下,向系统中充入1mol氮气后,平衡如何移动?
在100℃下,于装有NH3(g)的密封容器中放入过量的NH4Cl(s),NH4Cl(s)发生分解反应:
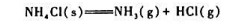
则系统的组分数C=(),相数P=(),自由度F=().
有固体AgBr(相对分子质量为187.8)0.1 g,能否完全溶解在100mL、1mol·L-1的氨水中?(已知[Ag(NH3)2]+的Kf=1.6×107,AgBr的Ksp=7.7×10-13)。
A.1, 2, 1
B.1, 2, 0
C.2, 2, 1
D.2, 2, 0
1mol H2O(1)在90℃。pθ下蒸发成同温同压的水蒸气,求此过程的△S,并判断此过程能否发生。已知90℃时水的饱和蒸气压为7.012×104Pa,H2O(1)的摩尔气化焓在90℃时为41.10kJ.mol-1、100℃时为40.66kJ.mol-1,H2O(1)和H2O(g)的摩尔恒压热容分别为75.40J.K-1.mol-1和33.58J.k-1.mol-1。水蒸气可近似作为理想气体。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
