 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
高温时NO2分解为NO和O2,其反应速率方程为 -v(NO2)=kc2(NO2) 在592K时,速率常数是4.98×10-1L·mol-1·s-1;
高温时NO2分解为NO和O2,其反应速率方程为
-v(NO2)=kc2(NO2)
在592K时,速率常数是4.98×10-1L·mol-1·s-1;在656K时,其值变为 4.74L·mol-1·s-1,计算该反应的活化能。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
高温时NO2分解为NO和O2,其反应速率方程为
-v(NO2)=kc2(NO2)
在592K时,速率常数是4.98×10-1L·mol-1·s-1;在656K时,其值变为 4.74L·mol-1·s-1,计算该反应的活化能。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“高温时NO2分解为NO和O2,其反应速率方程为 -v(NO2)=kc2(NO2) 在592K时,速率常数是4.98×10-1L·mol-1·s-1;”相关的问题
更多“高温时NO2分解为NO和O2,其反应速率方程为 -v(NO2)=kc2(NO2) 在592K时,速率常数是4.98×10-1L·mol-1·s-1;”相关的问题
NO2二聚反应的速率方程为-dc(NO2)/dt=kc2(NO2),会使速率常数发生变化的条件是( )。
(A) 将体系的总压力加倍
(B) 在反应混合物中加O2
(C) 在反应混合物中加过量NO2
(D) 在CCl4溶液中进行反应而不在气相中反应
在1073K时发生如下反应:2H2(g)+2NO(g)=N2(g)====2H2O(g)
为了确定反应的速率方程,通过配制一系列NO (g)与H2(g)浓度不同的混合物,测定反应起始速率,有关实验数据见下表,求该反应的速率方程。
H2(g)和NO(g)的反应速率(1073K)
| 实验标号 | 起始浓度/mol·dm-3 | 形成N2(g)的起始速率 /mol·dm-3·s-1 | |
| c(NO) | c(H2) | ||
| 1 2 3 4 5 6 | 6.0×10-3 6.0×10-3 6.0×10-3 1.0×10-3 2.0×10-3 3.0×10-3 | 1.0×10-3 2.0×10-3 3.0×10-3 6.0×10-3 6.0×10-3 6.0×10-3 | 3.19×10-3 6.36×10-3 9.56×10-3 0.48×10-3 1.92×10-3 4.30×10-3 |
对化学反应2NO(g)+O2(g)=2NO2(g),在下列各速率关系中正确的是()。
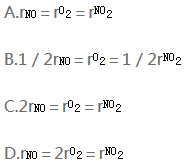
A. A
B. B
C. C
D. D
A、-2d[NO2]/dt = 2d[NO]/dt = d[O2]/dt
B、- d[NO2]/2dt = d[NO]/2dt = d[O2]/dt = dx/dt
C、- d[NO2]/2dt = d[NO]/2dt = d[O2]/dt = V-1 dx/dt
在600K时有反应2NO+O2→2NO2,NO和O2的初始浓度c(NO)和c(O2)及反应的初始速率υ的实验数据如下:
| c(NO)/(mol·L-1) | c(O2)/(mol·L-1) | υ/(mol·L-1·s-1) |
| 0.010 0.010 0.030 | 0.010 0.020 0.020 | 2.5×10-3 5.0×10-3 4.5×10-2 |
已知2N2O====4NO2+O2,反应机理如下:
N2O====NO2+NO3(快)
NO2+NO3====NO+O2+NO2(慢)
NO+NO3====2NO2(快)
该反应速率方程为______,它是一个______级反应

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
