 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知CO2在时的和0℃到1000℃的热容Cp,m,则CO2在1000K时的标准摩尔生成焓为(1000K)=+∫Cp,mdT。()
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有8位网友选择 错,占比80%
- · 有2位网友选择 对,占比20%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“已知CO2在时的和0℃到1000℃的热容Cp,m,则CO2在1000K时的标准摩尔生成焓为(1000K)=+∫Cp,mdT。()”相关的问题
更多“已知CO2在时的和0℃到1000℃的热容Cp,m,则CO2在1000K时的标准摩尔生成焓为(1000K)=+∫Cp,mdT。()”相关的问题
已知CO2(g)的摩尔定压热容
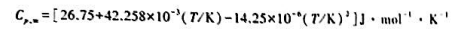
(1)求300K至800K间CO2(g)的平均摩尔定压热容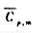 ;
;
(2)求1kg常压下的CO2(g)从300K恒压加热至800K时所需的热Q.
已知CH3COOH(g),CH4(g)和CO2(g)的平均摩尔定压热容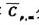 分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1.试由教材附录中三化合物的标准摩尔生成焓计算1000K时下列反应的
分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1.试由教材附录中三化合物的标准摩尔生成焓计算1000K时下列反应的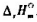 .
.
对于反应PbO(s)+CO(g)→Pb(s)+CO2(g),已知25℃的数据如表5-6所示。试求25℃时反应的KΘ。假定25~125℃间热容不变,求125℃时反应的KΘ。
表5-6
|
1
·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1试由附录中三化合物的标准摩尔生成焓计算1000K时下列反应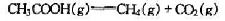 的
的
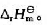
已知CH3COOH(g)、CO2(g)和CH4(g)的平均定压热容C ̅pm分别为52.3J.mol^-1.K^-1,
31.4J.mol^-1.K^-1,37.1J.mol^-1.K^-1。试由附录中各化合物的标准摩尔生成焓计算1000K时下列反应的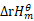 。
。
CH3COOH(g)=CH4(g)+C02(g)。
已知100kPa下冰的熔点为0℃,此时冰的比熔化焓△fush=333.3J·g-1。水的平均比定压热容cp为4.184J·g-1 ·K-1及2.000 J·g-1 ·K-1。求在绝热容器内向1kg50℃的水中投入0.1kg 0℃的冰后,系统末态温度。计算时不考虑容器的热容。
利用通用焓图求甲烷(CH4)由65MR70℃定压冷却到-6°C时放出的热量。
已知甲烷在理想气体状态下的摩尔定压热容为
将CO2(g)和CF4(g)的气体混合物通过1000℃的盛有铂催化剂的高温炉,将反应达到平衡后流出的气体冷却,取在0℃及标准压力时体积为524cm3的该气体与Ba(OH)2溶液反应,以全部吸收COF2及CO2:
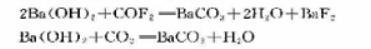
此时气相中剩余的CF4在0℃及标准压力下的体科为191cm3,再使Ba(OH)2溶液中的沉淀物与醋酸溶液共热,使碳酸盐溶解,余下不溶的BaF2固体,干燥后称重为1.0652g。试依据上述实验求算1000℃时反应2COF2(g)=CO2(g)+CF4(g)的Kθ。已知1000℃时,CO2(g)和CF4(g)的标准生成吉布斯自由能分别为-397.2kJ·mol-1和-489.3kJ·mol-1,试求该温度时COF2(g)的标准生成吉布斯自由能△rGmθ。
葡萄糖在空气中发生燃烧反应:

已知298.15K时空气中O2和CO2的分压分别为21.27kPa和0.0314kPa,
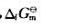 计算298.15K时该反应的摩尔吉布斯自由能变。
计算298.15K时该反应的摩尔吉布斯自由能变。
已知水蒸气性质如下,试估计水在600℃和0.8MPa时的等压热容和Joule-ThonlSon系数。
T/℃ | V/m3·kg-1 | H/kJ·kg-1 |
500 | 0.4433 | 3480.6 |
600 | 0.5018 | 3699.4 |
700 | 0.5601 | 3924.2 |

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
