 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


判断下列氧化还原反应在298.15 K时在标准状态下进行的方向:
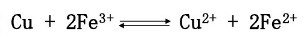
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)



 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“判断下列氧化还原反应在298.15 K时在标准状态下进行的方向:”相关的问题
更多“判断下列氧化还原反应在298.15 K时在标准状态下进行的方向:”相关的问题
A、501
B、2.0 ×10-3
C、2.7
D、-2.70
将氧化还原反应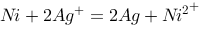 设计为一个原电池,已知
设计为一个原电池,已知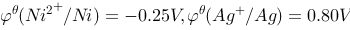 ,则原电池的电动势
,则原电池的电动势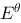 为1.05 (V),
为1.05 (V),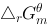 为-203 kJ/mol,该氧化还原反应的平衡常数为
为-203 kJ/mol,该氧化还原反应的平衡常数为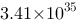 。
。

A、数值越大的电对氧化态的氧化能力越强。
B、数值越大的电对还原态的还原能力越强。
C、两个数值不同的电对可以构成原电池。
D、数值与介质无关
称取仅含弱酸盐NaA和NaB的Na2CO3试样0.6125g,加水溶解后,以甲基橙为指示剂,用浓度为0.2000mol/L HCl标准溶液滴定,甲基橙变色时,消耗HCl标准溶液32.72mL;上述等量样品加水溶解后,若以酚酞为指示剂,用0.1000mol/L HCl标准溶液滴定,消耗25.34mL。(1)写出有关反应方程式;(2)各组分的质量分数是多少?(已知:弱酸HA的pKa=7.0,弱酸HB的pKa=1,MNa2CO3=105.99,MNaA=182.03,MNaB=132.0)
A.由于s区元素的电负性小,所以都形成典型的离子型化合物
B.在s区元素中,Be和Mg因表面形成致密的氧化物保护膜而对水较稳定
C.s区元素的单质都有很强的还原性
D.除Be和Mg外,其他s区元素的硝酸盐或氯酸盐都可做焰火材料

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
