 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在pH=10.0的氨性溶液中,Mg2+和Hg2+的浓度分别为2.0×10-2mol·L-1和2×10-3mol·L-1,其中游离NaCN的浓度为2
已知在pH=10.0的氨性溶液中,Mg2+和Hg2+的浓度分别为2.0×10-2mol·L-1和2×10-3mol·L-1,其中游离NaCN的浓度为2.2×10-5mol·L-1。问在此条件下Hg2+能否被完全掩蔽?可否用同浓度的EDTA滴定其中的Mg2+?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)

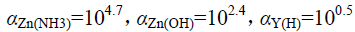 ,在此条件下,
,在此条件下,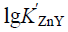 为( ) (已知
为( ) (已知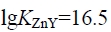 )
)




























