 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
正反应的活化能大于逆反应的活化能时,下列关于正反应的热效应的叙述中,正确的是()。
A.△rHm>0
B.△rHm<0<br>
C.△rHm=0.5*[Ea(正)-Ea(逆)]
D.△rHm=0.5*[Ea(正)+Ea(逆)]
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 C,占比44.44%
- · 有3位网友选择 D,占比33.33%
- · 有2位网友选择 A,占比22.22%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.△rHm>0
B.△rHm<0<br>
C.△rHm=0.5*[Ea(正)-Ea(逆)]
D.△rHm=0.5*[Ea(正)+Ea(逆)]
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“正反应的活化能大于逆反应的活化能时,下列关于正反应的热效应的叙述中,正确的是()。”相关的问题
更多“正反应的活化能大于逆反应的活化能时,下列关于正反应的热效应的叙述中,正确的是()。”相关的问题
A、DrHm=Ea’-Ea
B、DrHm=│Ea’-Ea│
C、DrHm=│Ea-Ea’│
D、DrHm=-(Ea’-Ea)
A、吸热反应的活化能大于放热反应的活化能
B、反应速率取决于所有反应物的浓度
C、对于可逆反应,催化剂只能改变正反应或逆反应的反应速率
D、速率常数k是反应物为单位浓度时的反应速率
(1)试结合图1.18.1所示的反应进程-势能图,定性判断该反应是吸热反应,还是放热反应,求算该反应的ΔtH;
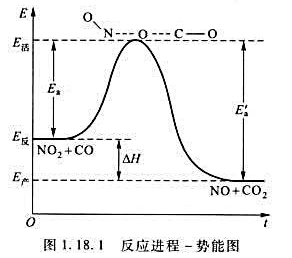
(2)若298K时的速率常数k=2.3×10-2s-1。试求373K时的速率常数;
(3)求算阿伦尼乌斯公式中的指前因子A。
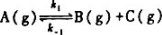 中,k1和k-1,在25℃时分别为0.2s-1和.3.9477x10-3MPa-1.s-1.在35℃时二者皆增为2倍.试求:
中,k1和k-1,在25℃时分别为0.2s-1和.3.9477x10-3MPa-1.s-1.在35℃时二者皆增为2倍.试求:(1)25C时的反应平衡常数Kθ;
(2)正、逆反应的活化能及25℃时的反应热Qm;
(3)若上述反应在25℃的恒容条件下进行,且A的起始压力为100kPa,若要使总压达到152kPa,问需要反应多长时间?
B、压缩体积,增大压力,平衡向右移动
C、升高温度,正反应速率增大,逆反应速率减小
D、加入催化剂,只增大正反应速率

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
