 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
乙酸乙酯皂化反应速率常数
在298 K时,测定乙酸乙酯皂化反应速率。反应开始时,溶液中酯和碱的浓度都为0.01mol·dm-3,每隔一定时间,用标准酸溶液滴定其中的碱含量,实验所得结果如下:

(1)证明该反应为二级反应,并求出速率常数k值;
(2)若酯和碱的起始浓度都为0.002mol·dm-3,试计算该反应完成95%时所需的时间及该反应的半衰期。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298 K时,测定乙酸乙酯皂化反应速率。反应开始时,溶液中酯和碱的浓度都为0.01mol·dm-3,每隔一定时间,用标准酸溶液滴定其中的碱含量,实验所得结果如下:

(1)证明该反应为二级反应,并求出速率常数k值;
(2)若酯和碱的起始浓度都为0.002mol·dm-3,试计算该反应完成95%时所需的时间及该反应的半衰期。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“乙酸乙酯皂化反应速率常数”相关的问题
更多“乙酸乙酯皂化反应速率常数”相关的问题
A、0.010mol·dm-3NaOH
B、0.005mol·dm-3NaOH
C、(C) 0.005mol·dm-3CH3COOH
D、0.005mol·dm-3CH3COONa
A、将乙酸乙酯和氢氧化钠同时加入大试管中立即进行测量即可。
B、将氢氧化钠溶液和等体积的水加入大试管中并恒温约10分钟后再测量。
C、将乙酸乙酯溶液和等体积的氢氧化钠溶液加入大试管内并恒温约10分钟后再测量。
D、将氢氧化钠溶液和等体积的水加入大试管中立即进行测量即可。
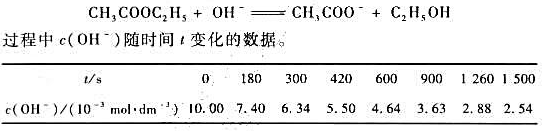
试计算最初180s时间内的平均反应速率和1260~1500s时间间隔内的平均反应速率,并说明二者大小不等的原因。
时间t(s) | NaOH(mol/L) | CH3COOC2H5(mol/L) |
0 | 0.5638 | 0.3114 |
393 | 0.4866 | 0.2342 |
669 | 0.4467 | 0.1943 |
1010 | 0.4113 | 0.1589 |
1265 | 0.3879 | 0.1354 |
A、乙酸乙酯皂化反应是二级反应
B、随着反应进行,溶液电导率不断下降
C、在此反应溶液中,CH3COONa是不完全电离的
D、体系的电导率值的减少量和CH3COONa的浓度增大成正比

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
