 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol单原子分子理想气体由始态(300K, 1 MPa), 经历如下途径膨胀到100 kPa; (1)等温可逆膨胀; (2)等温恒外压(100 kPa)膨胀; (3)向真空膨胀; (4)等外压(100 kPa)绝热膨胀, 求各过程的Q, W, DU, DH?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 更多“1mol单原子分子理想气体由始态(300K, 1 MPa), 经历如下途径膨胀到100 kPa; (1)等温可逆膨胀; (2)等温恒外压(100 kPa)膨胀; (3)向真空膨胀; (4)等外压(10…”相关的问题
更多“1mol单原子分子理想气体由始态(300K, 1 MPa), 经历如下途径膨胀到100 kPa; (1)等温可逆膨胀; (2)等温恒外压(100 kPa)膨胀; (3)向真空膨胀; (4)等外压(10…”相关的问题
1 mol 单原子理想气体的始态为300K 、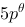 ,(1)在等温条件下向真空膨胀至
,(1)在等温条件下向真空膨胀至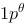 ,求此过程的Q,W, ΔU,ΔH,ΔS,ΔA,ΔG;(2)在等压条件下体积增至原来的2倍(V2=2V1),求过程的Q,W, ΔU,ΔH,ΔS。
,求此过程的Q,W, ΔU,ΔH,ΔS,ΔA,ΔG;(2)在等压条件下体积增至原来的2倍(V2=2V1),求过程的Q,W, ΔU,ΔH,ΔS。
组成为yB=O.6的单原子气体A与双原子气体B的理想气体混合物共10mol,从始态T1=300K,p1=50kPa,绝热可逆压缩至p2=200kPa的平衡态。求过程的W,△U,△H,△S(A)及△S(B)。
A.17.02kJ
B.-10.21kJ
C.-17.02kJ
D.10.21kJ
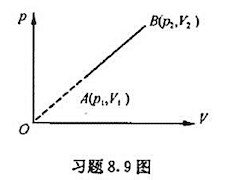
如附图所示,1mol的单原子分子理想气体从初态A(p1,V1)开始沿直线变到末态B(p2,V2)时,其内能的改变量为(),从外界吸热为(),对外界做功为()。
1mol 单原子分子理想气体,始态为 273 K,压力为p。分别经下列三种可逆变化,其Gibbs自由能的变化值各为多少? (1)恒温下压力加倍 (2)恒压下体积加倍 (3)恒容下压力加倍 假定在 273 K,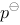 下,该气体的摩尔熵为
下,该气体的摩尔熵为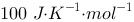
1mol理想气体在T=300K下,从始态100kPa经下列各过程,求Q,△S及△Siso。(1)可逆膨胀到末态压力50kPa;(2)反抗恒定外压50kPa不可逆膨胀至平衡态;(3)向真空自由膨胀至原体积的2倍。
1mol单原子理想气体,由温度为273K,体积为22.4dm3的始态,经由Ⅰ途径变化到温度为546K、体积仍为22.4dm3;再经由Ⅱ途径定温可逆膨胀至体积为44.8dm3;最后经由Ⅲ途径使系统定压回到其初态。试求出:
(1) 各状态下的气体压力;
(2) 系统经由各途径时的Q,W,△U,△H;
(3) 该循环过程的Q,W,△U,△H。
1mol单原子理想气体从300K加热至350K,(1)体积保持不变;(2)压强保持不变。问在这两过程中各吸收了多少热量?增加了多少内能?对外做了多少功?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
