题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在2Cu2++4I-=CuI↓+I2中,Eθ(I2/2I-)=54V,Eθ(Cu2+/CuI)=86V,Eθ(Cu2+/CuI)>Eθ(I2/2I-)则反应方向向()
A.右
B.左
C.不反应
D.反应达到平衡时不移动
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有3位网友选择 D,占比37.5%
- · 有2位网友选择 B,占比25%
- · 有2位网友选择 A,占比25%
- · 有1位网友选择 C,占比12.5%



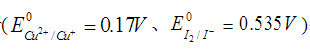 ;但若生成CuI沉淀后情况会有所变化。通过计算判定(均在标准状态下)2Cu2++4I-→2CuI↓+I2↓反应的方向
;但若生成CuI沉淀后情况会有所变化。通过计算判定(均在标准状态下)2Cu2++4I-→2CuI↓+I2↓反应的方向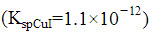 ()。
()。