 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在1.013×105Pa下测得N2O4(g)在60℃时有50%离解,计算反应N2O4(g)2NO2(g)的Kp。
在1.013×105Pa下测得N2O4(g)在60℃时有50%离解,计算反应N2O4(g) 2NO2(g)的Kp。
2NO2(g)的Kp。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在1.013×105Pa下测得N2O4(g)在60℃时有50%离解,计算反应N2O4(g) 2NO2(g)的Kp。
2NO2(g)的Kp。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“在1.013×105Pa下测得N2O4(g)在60℃时有50%离解,计算反应N2O4(g)2NO2(g)的Kp。”相关的问题
更多“在1.013×105Pa下测得N2O4(g)在60℃时有50%离解,计算反应N2O4(g)2NO2(g)的Kp。”相关的问题
反应:2N2O5(g)====4NO2(g)+O2(g)
起始时N2O5(g)浓度为1.15mol·dm-3,100s后测得N2O5(g)浓度为1.0mol·dm-3,则反应在100s内的平均速率为多少?
已知E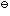 (Zn2+/Zn)= -0.763V,E
(Zn2+/Zn)= -0.763V,E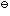 (Ni2+/Ni)= -0.25V。将下列反应:Zn(s)+Ni2+(aq)
(Ni2+/Ni)= -0.25V。将下列反应:Zn(s)+Ni2+(aq) Zn2+(aq)+Ni(s)构成一原电池,测得电动势为0.54V,且c(Ni2+)=1.0mol·L-1,则此时c(Zn2+)为()。
Zn2+(aq)+Ni(s)构成一原电池,测得电动势为0.54V,且c(Ni2+)=1.0mol·L-1,则此时c(Zn2+)为()。
A、0.020mol·L-1
B、0.320mol·L-1
C、0.500mol·L-1
D、0.12mol·L-1
有一个如图所示的平行板电容器,若在两极板间充满电容率为
![]() 的电介质,两板接在电压为U0的直流电源上,忽略边缘效应,求两极板间的电场E,电位移D,极化强度p及极化体电荷密度ρp和极化面电荷密度σp。
的电介质,两板接在电压为U0的直流电源上,忽略边缘效应,求两极板间的电场E,电位移D,极化强度p及极化体电荷密度ρp和极化面电荷密度σp。
![]()

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
