 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算CaCO3在水中的溶解度。用300mL水洗涤含有0.300g CaCO3的沉淀,会有多少克CaCO3被溶解?其损失的相对误差是
计算CaCO3在水中的溶解度。用300mL水洗涤含有0.300g CaCO3的沉淀,会有多少克CaCO3被溶解?其损失的相对误差是多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算CaCO3在水中的溶解度。用300mL水洗涤含有0.300g CaCO3的沉淀,会有多少克CaCO3被溶解?其损失的相对误差是多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“计算CaCO3在水中的溶解度。用300mL水洗涤含有0.300g CaCO3的沉淀,会有多少克CaCO3被溶解?其损失的相对误差是”相关的问题
更多“计算CaCO3在水中的溶解度。用300mL水洗涤含有0.300g CaCO3的沉淀,会有多少克CaCO3被溶解?其损失的相对误差是”相关的问题
25℃时,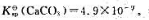 试计算:
试计算:
(1)25℃时CaCO3(s)在水中的溶解度;
(2)25℃时CaCO3(s)在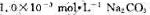 液中的溶解度。
液中的溶解度。
钙离子主要来自于地层中的石灰石(CaCO3)和石膏(CaSO4•2H2O)。CaCO3在水中的溶解度虽然很小,但在水中含有二氧化碳CO2时,它就比较易溶解。这是因为它们相互反应生成溶解度较大的碳酸氢钙CaHCO3-的缘故。()
298 K,Ksp,CaCO3=8.7×10-9,CaCO3在水中的溶解度为()。
A.9.3×10-5mol·L-1
B.8.7×10-9mol·L-1
C.8.7×10-5mol·L-1
D.4.4×10-5mol·L-1
常温常压下,CO2在水中的溶解度为0.033mol•dm-3,求该条件下CaCO3在饱和CO2水溶液中的溶解度。已知CaCO3的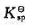 =2.8x10^-9,H2CO3的K1=4.5x10^-7,K2=4.7x10^-11。
=2.8x10^-9,H2CO3的K1=4.5x10^-7,K2=4.7x10^-11。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
