 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试设计一个电池,使其中进行下述反应:(1)写出电池表示式;(2)计算25℃时,上述电池反应的Kθ
试设计一个电池,使其中进行下述反应:

(1)写出电池表示式;
(2)计算25℃时,上述电池反应的Kθ;
(3)若将过量的银粉加到浓度为0.05mol·kg-1的Fe(NO3)3溶液中,求反应达平衡后Ag+的浓度为多少?(设活度系数均为1).已知φθ(Fe3+|Fe2+)=0.771V,φθ(Ag|Ag+)=0.7991V.
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)

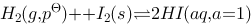 (1)写出电池表达式 (2)计算上述反应在 298 K 时的
(1)写出电池表达式 (2)计算上述反应在 298 K 时的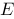 、
、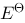 、
、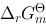 和
和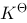 (3)若反应写成
(3)若反应写成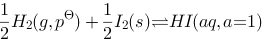 则
则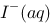 的Gibbs生成自由能
的Gibbs生成自由能 。
。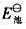 ,再计算电池反应的
,再计算电池反应的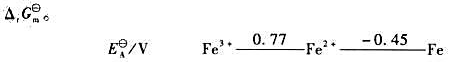
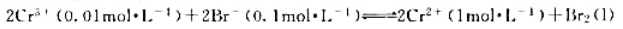
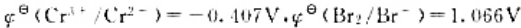
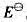 。
。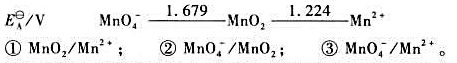
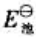 和电池反应的
和电池反应的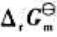 。
。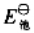 和电池反应的
和电池反应的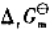 。
。




























