 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用对比的方法说明以下概念的区别:(1)原子与分子(2)原子与元素(3)核素与元素(4)单质与化合物(5)同位素与同素异形体(6)核素与同位素(7)分子式与化学式(8)化学式式量与分子量(9)原子量与原子质量
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“用对比的方法说明以下概念的区别:(1)原子与分子(2)原子与元素(3)核素与元素(4)单质与化合物(5)同位素与同素异形体(6)核素与同位素(7)分子式与化学式(8)化学式式量与分子量(9)原子量与原…”相关的问题
更多“用对比的方法说明以下概念的区别:(1)原子与分子(2)原子与元素(3)核素与元素(4)单质与化合物(5)同位素与同素异形体(6)核素与同位素(7)分子式与化学式(8)化学式式量与分子量(9)原子量与原…”相关的问题
A.同一元素各核素的质量数不同,但它们的化学性质几乎完全相同
B.任何元素的原子都是由核外电子和核内中子、质子组成的
C.核素指一种原子,而元素是指一类原子;核素间互称同位素,元素包含同位素
D.的质量数相同,所以它们是互为同位素
E.钠原子失去一个电子后,它的电子数与氖原子相同,所以变成氖原子
试区别下列各术语:
(1)基态原子与激发态原子;
(2)概率与概率密度;
(3)原子轨道与电子云:
(4)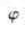 与
与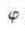 2
2
A.原子最外层电子数为2的元素一定处于周期表的第IIA族
B.构成单质的分子中一定含有共价键
C.同主族元素形成的氧化物的晶体类型均相同
D.金属与非金属元素形成的化合物可能是离子化合物
A、1:1
B、4:1
C、1:2
D、1:4
| (14分)下表所示的是第二周期元素中,除Be、B、Ne三种元素外,其它元素的简单氢化物的沸点;题26图所示是第三周期元素中,除Ar以外的其它元素的单质的熔点变化关系。
(1)X的简单氢化物属于____分子(填“极性”或“非极性”),G元素的单质在固态时的晶体类型为________。 (2)写出W的氢化物的电子式__________。 (3)A和Z两元素形成的一种化合物分子中各原子最外均达到8电子稳定结构,则该分子的结构式为____。 (4)化合物AY能与水反应生成两种弱酸,其化学方程式为____ (5)写出元素F的单质与三氧化二铬反应的化学方程式_______ |
A.在一般的单质中,元素原子的氧化数指定为0
B.在一般化合物中,氢原子的氧化数指定是+1
C.氧原子的氧化数指定是-2
D.在中性分子中,各元素原子氧化素的代数和是0
判断下列各对元素中哪一种元素的第一电离能大,并说明原因。
(1) S与P; (2) Al与Mg; (3) Sr与Rb; (4) Cu与Zn; (5) Cs与Au。
A.具有相同核电荷数的同一类原子称为元素
B.具有相同质子数、中子数和核能态的一类原子称为核素
C.质子数相同中子数不同的一类核素称为同位素
D.一种元素可包括多种同位素
E.核反应是指原子核与原子核之间或原子核与其他粒子之间的相互作用

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
