 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
起始浓度分别为c1和c2的分子电解质刚果红NaR与KCl溶液分布在半透膜两边,其膜平衡条件是什么?
A.[K+]内/[K+]外=[Na]内/[Na]外=[Cl]外/[Cl]内
B.[Na]内[Cl]内=[Na]外[Cl]外
C.[K]内[Cl]内=[K]外[Cl]外
D.[Na]内[Cl]内+[K]内[Cl]内=[Na]外[Cl]外+[K]外[Cl]外
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有5位网友选择 A,占比62.5%
- · 有2位网友选择 C,占比25%
- · 有1位网友选择 B,占比12.5%



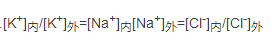
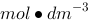 ) 如下(膜两侧溶液体积相等):
) 如下(膜两侧溶液体积相等):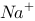
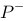

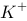

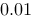
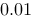

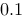
 其中
其中




























