 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友wma1102
发布时间:2022-12-29
[主观题]
HF的σ成键分子轨道可表示为∮HF=c1,H原子的1s轨道能为-13.6eV,F的2p轨道能为-17.4eV,则c1、c2组合
HF的σ成键分子轨道可表示为∮HF=c1
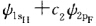 ,H原子的1s轨道能为-13.6eV,F的2p轨道能为-17.4eV,则c1、c2组合系数哪个大?c12、c22分别表示什么?
,H原子的1s轨道能为-13.6eV,F的2p轨道能为-17.4eV,则c1、c2组合系数哪个大?c12、c22分别表示什么?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
根据分子轨道理论两个能量不同的原子轨道组合成两个分子轨道时成键分子轨道中含能量较低的原子轨道成分多反键轨道中含能量较高的原子轨道成分多。F的2pz轨道能低于H的1s轨道能故|c2|>|c1|。c12和c22分别表示H的1s轨道和F的2pz轨道对HF成键分子轨道的贡献。
根据分子轨道理论,两个能量不同的原子轨道组合成两个分子轨道时,成键分子轨道中含能量较低的原子轨道成分多,反键轨道中含能量较高的原子轨道成分多。F的2pz轨道能低于H的1s轨道能,故|c2|>|c1|。c12和c22分别表示H的1s轨道和F的2pz轨道对HF成键分子轨道的贡献。
根据分子轨道理论,两个能量不同的原子轨道组合成两个分子轨道时,成键分子轨道中含能量较低的原子轨道成分多,反键轨道中含能量较高的原子轨道成分多。F的2pz轨道能低于H的1s轨道能,故|c2|>|c1|。c12和c22分别表示H的1s轨道和F的2pz轨道对HF成键分子轨道的贡献。

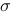 轨道和
轨道和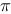 轨道分别有 条和 条。
轨道分别有 条和 条。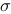 轨道和
轨道和 轨道分别有 条和 条。
轨道分别有 条和 条。





























