 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用氧化还原法测定钡的含量时,先将Ba2+沉淀为Ba(IO3)2,过滤,洗涤后溶解于酸,加入过量KI,析出的I2用Na2S2O3标
用氧化还原法测定钡的含量时,先将Ba2+沉淀为Ba(IO3)2,过滤,洗涤后溶解于酸,加入过量KI,析出的I2用Na2S2O3标准溶液滴定,则BaCl2与Na2S2O3的物质的量之比是多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用氧化还原法测定钡的含量时,先将Ba2+沉淀为Ba(IO3)2,过滤,洗涤后溶解于酸,加入过量KI,析出的I2用Na2S2O3标准溶液滴定,则BaCl2与Na2S2O3的物质的量之比是多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“用氧化还原法测定钡的含量时,先将Ba2+沉淀为Ba(IO3)2,过滤,洗涤后溶解于酸,加入过量KI,析出的I2用Na2S2O3标”相关的问题
更多“用氧化还原法测定钡的含量时,先将Ba2+沉淀为Ba(IO3)2,过滤,洗涤后溶解于酸,加入过量KI,析出的I2用Na2S2O3标”相关的问题
A、2∶1
B、12∶1
C、3∶1
D、6∶1
用氧化还原法测定钡的含量时,先将 沉淀为
沉淀为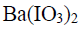 过滤,洗涤后溶解于酸,加入过量KI,析出的
过滤,洗涤后溶解于酸,加入过量KI,析出的 用
用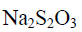 标准溶液滴定,则
标准溶液滴定,则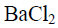 与
与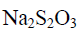 的物质的量之比为( )
的物质的量之比为( )
A、1:2
B、1:12
C、1:3
D、1:16
用沉淀重量法测定矿石中的铁含量,称量式为Fe2O3,若以Fe表示矿石中铁含量,则换算因数为()
A. 0.699
B. 0.350
C. 0.966
D. 0.450
用KMnO4法测定某污染物中的Fe时,称取试样0.5000g,滴定用去0.04000mol·L-1KMnO4溶液35.22mL。因为滴定时不慎超过终点,所以用了1.23mL FeSO4回滴,已知每毫升FesO4相当于0.88mLKMnO4。求该污染物中铁的含量。[M(Fe)=55.85g·mol-1]
用间接滴定法测定软锰矿中的MnO2时,先加入过量的HCl,将生成的Cl2通入KI溶液中,最后用Na2S2O3滴定生成的I2,则MnO2与Na2S2O3的计量关系是多少?
H2NNH2+2I2====4I-+N2↑+4H+
再用过量的Br2氧化,除去剩余的Br2后加入过量KI,酸化,以淀粉作指示剂,用Na2S2O3标准溶液滴定,求得I-的含量。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
