 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


分别计算0.100mol·L-1KMnO4和0.100mol·L-1K2Cr2O7在H+浓度为1.0mol·L-1介质中,还原一半时的电势。计算结果说
分别计算0.100mol·L-1KMnO4和0.100mol·L-1K2Cr2O7在H+浓度为1.0mol·L-1介质中,还原一半时的电势。计算结果说明什么?(已知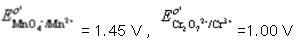 。)
。)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


分别计算0.100mol·L-1KMnO4和0.100mol·L-1K2Cr2O7在H+浓度为1.0mol·L-1介质中,还原一半时的电势。计算结果说明什么?(已知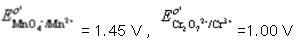 。)
。)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“分别计算0.100mol·L-1KMnO4和0.100mol·L-1K2Cr2O7在H+浓度为1.0mol·L-1介质中,还原一半时的电势。计算结果说”相关的问题
更多“分别计算0.100mol·L-1KMnO4和0.100mol·L-1K2Cr2O7在H+浓度为1.0mol·L-1介质中,还原一半时的电势。计算结果说”相关的问题
1.0×10-3mol·L-1的K2Cr2O7溶液在波长450nm和530nm处的吸光度A分别为0.200和0.050。1.0×10-4mol·L-1的KMnO4溶液在450nm450nm和530nm处的吸光度分别为0.380和0.710。试计算该混合溶液中K2Cr2O7和KMnO4的浓度。假设吸收池厚度为10mm。
称取含Cr和Mn的钢样0.8000g,经处理后,得到Fe3+、Cr2O2-7和Mn2+溶液。在F-存在时,用0.005000mol/LKMnO4标准滴定溶液滴定,此时Mn(Ⅱ)变成Mn(Ⅲ),用去KMnO4溶液20.00mL。然后将此溶液继续用0.04000mol/LFe2+标准滴定溶液滴定,用去30.00mL。则试样中Cr和Mn的含量分别为()。已知M(Cr)=51.996g/mol,M(Mn)=54.94g/mol。
A. 5.50%和3.04%
B. 2.75%和1.52%
C. 1.52%和2.75%
D. 3.04%和5.50%
称取含MnO、Cr2O3的矿样1.000g,用Na2O2熔融后,用水浸取,得到Na2MnO4和Na2CrO4溶液。煮沸溶液以除去过氧化物。酸化溶液,此时MnO42-歧化为MnO4-和MnO2。滤去MnO2。滤液中加入25.00mL0.1000mol·L-1Fe2+溶液,过量的Fe2+用10.000mL0.01000mol·L-1KMnO4溶液返滴定。沉淀用10.00mL0.1000mol·L-1Fe2+溶液处理,过量的Fe2+用14.20mL0.01000mol·L-1KMnO4溶液返滴定。求矿样中MnO和Cr2O3的含量。[M(MnO)=70.94g·mol-1,M(Cr2O3)=152.0g·mol-1]
计算题:配制500mLC(H2SO4)2mol/L的稀H2SO4需要多少毫升C(H2SO4)16mol/L的H2SO4?
A、Tirso de Molina
B、Pedro Calderón de la Barca
C、Lope de Vega
D、Fray Luis de Léon
A、可用直接法配制标准溶液
B、K2Cr2O7标准溶液非常稳定,便于长期保存
C、室温下Cl-不干扰测定
D、需采用二苯胺磺酸钠指示剂

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
