 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若已知下列电对电极电势的大小顺序:j(F2/F-) >j(Fe3+/Fe2+) >j(Mg2+/Mg) >j(Na+/Na)则下列离子中最强的还原剂是
A.F-
B.Fe2+
C.Na+
D.Mg2+
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 C,占比44.44%
- · 有4位网友选择 D,占比44.44%
- · 有1位网友选择 B,占比11.11%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.F-
B.Fe2+
C.Na+
D.Mg2+
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“若已知下列电对电极电势的大小顺序:j(F2/F-) >j(Fe3+/Fe2+) >j(Mg2+/Mg) >j(Na+/Na)则下列离子中最强的还原剂是”相关的问题
更多“若已知下列电对电极电势的大小顺序:j(F2/F-) >j(Fe3+/Fe2+) >j(Mg2+/Mg) >j(Na+/Na)则下列离子中最强的还原剂是”相关的问题

A、MnO42->MnO2 >Mn2+
B、MnO2 > MnO42->Mn2+
C、MnO42- >Mn2+ > MnO2
D、Mn2+ > MnO2 > MnO42-
A、非自发的
B、处于平衡态
C、自发的
D、无法判断
已知298.15K时,φ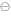 (Fe
(Fe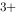 / Fe
/ Fe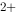 )=0.771V,φ
)=0.771V,φ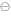 (Ag
(Ag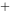 / Ag)=0.7996V,则Ag+Fe
/ Ag)=0.7996V,则Ag+Fe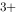 =Ag
=Ag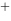 +Fe
+Fe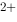 的标准平衡常数为( )。
的标准平衡常数为( )。
A、3.042
B、0.3288
C、1.623
D、3.623
A、Fe3+和Cl-
B、Fe3+和Hg22+
C、Cr2O72-和Cl-
D、Cr2O72-和Fe2+
A、E(Fe3+/ Fe2+)> E(I2/ I-)> E(Br2/ Br -)
B、E(I2/ I-)> E(Fe3+/ Fe2+)> E(Br2/ Br -)
C、E(Br2/ Br -)> E(I2/ I-)> E(Fe3+/ Fe2+)
D、E(Br2/ Br -)> E(Fe3+/ Fe2+)> E(I2/ I-)
 。
。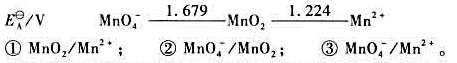
(2)试写出以电对①为负极、电对②为正极的原电池的电池反应,并计算原电池的标准电动势 和电池反应的
和电池反应的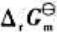 。
。
(3)试写出以电对①为负极、电对③为正极的原电池的电池反应,并计算原电池的标准电动势 和电池反应的
和电池反应的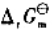 。
。
298.15K标准状态下,反应[Cu(CN)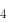 ]
]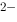 +4H
+4H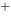 = 4HCN + Cu
= 4HCN + Cu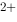 自发进行的方向应为( )。(已知298.15K时,
自发进行的方向应为( )。(已知298.15K时,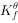
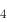 ]
]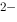 }=2.0×10
}=2.0×10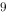 ,
,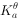
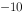 )
)
A、正向
B、逆向
C、平衡
D、三种情况都有可能

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
