 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列关于乙烯分子的成键情况,分析正确的是:
A.每个C原子的2s轨道与2p轨道杂化,形成两个sp杂化轨道
B.
C.
D.每个C原子的3个价电子占据3个杂化轨道,1个价电子占据1个2p轨道
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有3位网友选择 C,占比37.5%
- · 有2位网友选择 A,占比25%
- · 有2位网友选择 B,占比25%
- · 有1位网友选择 D,占比12.5%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.每个C原子的2s轨道与2p轨道杂化,形成两个sp杂化轨道
B.
C.
D.每个C原子的3个价电子占据3个杂化轨道,1个价电子占据1个2p轨道
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“下列关于乙烯分子的成键情况,分析正确的是:”相关的问题
更多“下列关于乙烯分子的成键情况,分析正确的是:”相关的问题
A.每个C原子的2s轨道与2p轨道杂化,形成两个sp杂化轨道
B.每个C原子的1个2s轨道与2个2p轨道杂化,形成3个sp2杂化轨道
C.每个C原子的2s轨道与3个2p轨道杂化,形成4个sp3杂化轨道
D.每个C原子的3个价电子占据3个杂化轨道,1个价电子占据1个2p轨道
A.碳碳三键的杂化方式是sp杂化,其中两个p轨道相互交盖形成一个碳-碳σ键,另外两个sp杂化轨道互相交盖形成π键
B.碳碳三键的杂化方式是sp杂化,其中两个sp杂化轨道相互交盖形成一个碳-碳σ键,另外每个碳原子剩下的两个p轨道与另一个碳原子的两个p轨道互相交盖形成两个互相垂直的π键
C.碳碳三键的杂化方式是sp杂化,其中两个sp杂化轨道相互交盖形成一个碳-碳σ键,另外每个碳原子剩下的两个p轨道与另一个碳原子的两个p轨道互相交盖形成两个互相平行的π键
D.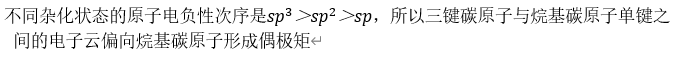
PCl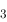 分子中,P与Cl成键采用的轨道是()。
分子中,P与Cl成键采用的轨道是()。
A、p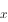 ,p
,p 及p
及p 轨道
轨道
B、三个sp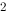 杂化轨道.
杂化轨道.
C、两个sp杂化轨道与一个p轨道
D、三个不等性sp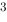 杂化轨道
杂化轨道
A.它是由一个1s轨道和一个2p轨道线性组合而成
B.等性sp杂化轨道中所含s、p的成分一样
C.等陛sp杂化轨道有两个,一个能量升高,另一个能量降低,但总能量保持不变
D.等性sp杂化轨道可与其他原子轨道形成σ键和π键
PCl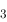 分子中,P与Cl成键采用的轨道是()。
分子中,P与Cl成键采用的轨道是()。
A、p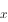 ,p
,p 及p
及p 轨道
轨道
B、三个sp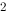 杂化轨道.
杂化轨道.
C、两个sp杂化轨道与一个p轨道
D、三个不等性sp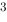 杂化轨道
杂化轨道
A.原子在基态没有未成对电子,则不能形成共价键
B.分子的几何构型取决于中心原子的杂化轨道数目
C.sp2杂化轨道是由某个原子的1s和2p轨道杂化而成的
D.一般杂化轨道的成键能力比参与杂化的原子轨道的成键能力强

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
