 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友p444y888
发布时间:2022-01-06
[主观题]
活化能的大小不一定反映了一个化学反应的快慢,但可反映反应速率常数受温度影响的大小。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
查看官方参考答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“活化能的大小不一定反映了一个化学反应的快慢,但可反映反应速率常数受温度影响的大小。”相关的问题
更多“活化能的大小不一定反映了一个化学反应的快慢,但可反映反应速率常数受温度影响的大小。”相关的问题
(A) 化学反应动力学是研究反应的快慢和限度的;
(B) 反应速率常数大小即是反应速率的大小;
(C) 反应级数越大,反应速率越大;
(D) 活化能的大小不一定总能表示一个反应的快慢,但可表示反应速率常数受温度影响的大小。
对行反应A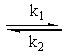 B,当温度一定时由纯A开始反应,下列说法中错误的是:
B,当温度一定时由纯A开始反应,下列说法中错误的是:
A、开始时A的消耗速率最快
B、反应的净速率是正、逆向反应速率之差
C、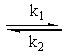 值是恒定的
值是恒定的
D、达到平衡时正、逆向的反应速率系数相等
燃煤活化能及频率因子
| 煤 种 | Vdaf(%) | k0[g/(cm2·s·MPa)] | E(kJ/mol) |
| 无烟煤 | 5.15 | 96.83 | 85.212 |
| 贫煤 | 15.18 | 12.61 | 55.098 |
| 烟煤 | 33.4 | 7.89 | 45.452 |
| 褐煤 | 41.02 | 5.31 | 38.911 |
A、发生反应的活化能越小,反应速率增加越大
B、增大系统压力,反应速率增大
C、加入催化剂,使正反应活化能和逆反应活化能变化的倍数相同
D、反应速率常数k是温度的函数,是一个有量纲的物理量

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
