 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
两个半电池,电极相同,电解质溶液中的物质也相同,都可以进行电极反应,但溶液的浓度不同,它们组成电池的电动势
A.
B.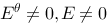
C.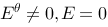
D.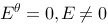
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 D,占比50%
- · 有2位网友选择 B,占比25%
- · 有1位网友选择 A,占比12.5%
- · 有1位网友选择 C,占比12.5%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.
B.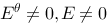
C.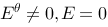
D.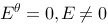
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“两个半电池,电极相同,电解质溶液中的物质也相同,都可以进行电极反应,但溶液的浓度不同,它们组成电池的电动势”相关的问题
更多“两个半电池,电极相同,电解质溶液中的物质也相同,都可以进行电极反应,但溶液的浓度不同,它们组成电池的电动势”相关的问题
A.Ef = 0, E = 0
B.Ef ≠ 0, E≠ 0
C.Ef ≠ 0, E = 0
D.Ef = 0, E≠ 0
A.标准电动势为0,电动势不为0
B.标准电动势不为0,电动势不为0
C.标准电动势为0,电动势为0
D.标准电动势为0,电动势不为0
A.∆E0=0, ∆E=0
B.∆E0 ≠0,∆E ≠0
C.∆E0≠0, ∆E=0
D.∆E0=0,∆E ≠0
浓差电池的两个电极由金属X所组成,一个电极浸入浓度为0.5mol·dm-3相应的盐溶液中,另一个浸入浓度为0.05mol·dm-3相同盐的溶液中,298K时该电池的电动势为0.028v,请计算X的价数。
下列说法是否正确?为什么? 1.相同浓度的HCl,KCl和NaCl三种溶液中Cl-的迁移数相同。 2.根据摩尔电导率的定义,溶液中能导电的电解质的物质的量已经给定,因此,摩尔电导率与溶液的浓度无关。 3.若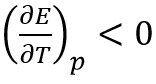 ,则 ΔS< 0,因此该电池反应不能自发进行。 4.对一个指定的电极,当电极反应的写法不同时,电极电势也不同。 5.恒温恒压下,指定原电池分三种情况放电: (1)电流等于零;(2)电流大于零;(3)电池短路。 在上述三种情况下,电池的电动势不相同。
,则 ΔS< 0,因此该电池反应不能自发进行。 4.对一个指定的电极,当电极反应的写法不同时,电极电势也不同。 5.恒温恒压下,指定原电池分三种情况放电: (1)电流等于零;(2)电流大于零;(3)电池短路。 在上述三种情况下,电池的电动势不相同。
已知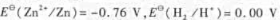 ,用两个电极组成原电池,电池符号为
,用两个电极组成原电池,电池符号为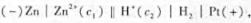 ,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势为-0.80 V, 则锌电极中锌离子的浓度c1=()Mol· L-1,氢电极的电极电势E(H2/H+)=()。 氢半电池中氢离子的浓度c2=()mol· L-1,氢半电池中溶液的pH=().该氧化还原反应达到平衡时,反应的
,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势为-0.80 V, 则锌电极中锌离子的浓度c1=()Mol· L-1,氢电极的电极电势E(H2/H+)=()。 氢半电池中氢离子的浓度c2=()mol· L-1,氢半电池中溶液的pH=().该氧化还原反应达到平衡时,反应的 。
。
下列说法是否正确?为什么? 1.相同浓度的HCl,KCl和NaCl三种溶液中Cl-的迁移数相同。 2.根据摩尔电导率的定义,溶液中能导电的电解质的物质的量已经给定,因此,摩尔电导率与溶液的浓度无关。 3.若 ,则 ΔS< 0,因此该电池反应不能自发进行。 4.对一个指定的电极,电极电势的值与电极反应的写法无关。 5.恒温恒压下,指定原电池分三种情况放电: (1)电流等于零;(2)电流大于零;(3)电池短路。 在上述三种情况下,电池的电动势不相同。
,则 ΔS< 0,因此该电池反应不能自发进行。 4.对一个指定的电极,电极电势的值与电极反应的写法无关。 5.恒温恒压下,指定原电池分三种情况放电: (1)电流等于零;(2)电流大于零;(3)电池短路。 在上述三种情况下,电池的电动势不相同。
在各种不同的电解质溶液中,通过相同的电荷量时,每个电极上电极反应产物的(质)量与它们的______成正比。
产生浓差极化的原因是()
A.两个半电池中溶液浓度的不同
B.电极附近和溶液内部电解质浓度的改变
C.电池的可逆性
D.测量时温度的变化

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
