 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友18***590
发布时间:2022-05-25
[主观题]
用s,p,d,f等符号表示下列元素的原子电子层结构(原子电子构型),判断它们属于第几周期、第几主族
用s,p,d,f等符号表示下列元素的原子电子层结构(原子电子构型),判断它们属于第几周期、第几主族
或副族.
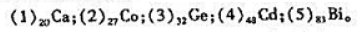
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
查看官方参考答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
或副族.
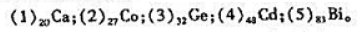
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“用s,p,d,f等符号表示下列元素的原子电子层结构(原子电子构型),判断它们属于第几周期、第几主族”相关的问题
更多“用s,p,d,f等符号表示下列元素的原子电子层结构(原子电子构型),判断它们属于第几周期、第几主族”相关的问题
试用S、P、d、f符号来表示下列各元素原子的电子层结构。
(1)18Ar;(2)26Fe;(3)53I;(4)47Ag。
并指出它们各属于第几周期?第几族?
已知下列元素原子的价层电子构型为
(1)3s2;(2)4s24p1;(3)3d54s2;(4)3d104s2。
它们分别属于第几周期?第几族?哪个区?最高氧化值是多少?
已知四种元素的原子的外层电子层结构分别为:
(1)4s2;(2)3s23p5;(3)3d24s2;(4)5d106s2。
试指出它们在周期系中各处于第几周期?第几族?哪个区?
已知某元素原子的外层电子构型为3d104s2,试写出其电子构型、原子序数,判断是几周期?什么区?几族?主族还是副族?金属还是非金属元素?是什么元素?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
