 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列物质中,属于共价化合物的是
A、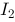
B、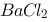
C、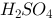
D、NaOH
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、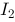
B、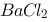
C、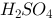
D、NaOH
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 更多“下列物质中,属于共价化合物的是”相关的问题
更多“下列物质中,属于共价化合物的是”相关的问题
指出下列物质中是离子化合物有______,共价化合物有_______,极性分子有______,非极性分子有______。
SO2HgCl2H2S KBr HI CCl4NF3CS2
A.离子化合物中可以含有共价键,但共价化合物中一定不含离子键
B.含有共价键的物质一定是共价化合物
C.H 2 O稳定是因为H 2 O中存在两个氢键
D.干冰升华时,分子内共价键会发生断裂
A.熔化状态下能导电的物质一定是离子化合物
B.离子化合物均能溶于水
C.离子化合物不可能由非金属元素组成
D.共价化合物中一定不含离子键
下列物质中,指出哪些是离子型化合物、共价化合物、极性分子、非极性分子?
KBr KI CS2(直线形) SO2(角折形) CCl4(正四面体)
H2S(角折形) HgCl2(直线形) NF3(三角锥形)
A.在离子晶体不可能存在非极性键
B.共价化合物中不可能存在离子键
C.共价化合物中可能存在离子键,也可能存在非极性键和极性键
D.含有共价键的化合物一定不是离子化合物
下列化合物中共价性最强的是
(A) LiI; (B) CsI; (C) BeI2; (D) MgI2。
A.HCl属于共价化合物,溶于水能电离出H+和Clˉ
B.NaOH是离子化合物,该物质中只含有离子键
C.HI气体受热分解的过程中,只需克服分子间作用力
D.石英和干冰均为原子晶体

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
