题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
关于周期表与周期律,下列说法哪一种是正确的A、元素的性质随着原子量的递增,呈周期性变化B、在周期
关于周期表与周期律,下列说法哪一种是正确的
A、元素的性质随着原子量的递增,呈周期性变化
B、在周期表中,族序数都等于该元素的原子的最外层电子数
C、在周期表中,非金属性最强的元素,其最高价氧化物对应水化物的酸性也最强
D、随着核电荷数的递增,元素原子半径依次增大
E、IA族单质自上而下,随原子量的增大,溶沸点降低
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)

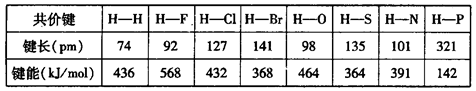
 2NaH)。生成物氢化钠的电子式为__________,含有的化学键为_______键(填“离子”、“共价”或“金属”)。
2NaH)。生成物氢化钠的电子式为__________,含有的化学键为_______键(填“离子”、“共价”或“金属”)。