 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若计算得到电池反应的电池电动势为负值,表示此电池反应是。
A.正向进行
B.逆向进行
C.不可能进行
D.反应方向不确定
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有2位网友选择 C,占比25%
- · 有2位网友选择 D,占比25%
- · 有2位网友选择 A,占比25%
- · 有2位网友选择 B,占比25%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.正向进行
B.逆向进行
C.不可能进行
D.反应方向不确定
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“若计算得到电池反应的电池电动势为负值,表示此电池反应是。A、正向进行B、逆向进行C、不可能进行D”相关的问题
更多“若计算得到电池反应的电池电动势为负值,表示此电池反应是。A、正向进行B、逆向进行C、不可能进行D”相关的问题
若算得电池反应的电池电动势为负值时,表示此电池反应是:
(A) 正向进行 (B) 逆向进行 (C) 不可能进行 (D) 反应方向不确定
用能斯特公式算得电池的电动势为负值,表示此电池反应的方向是朝______进行(选填“正向”、“逆向”)。
A.电极极化就是电极的电极电位偏离了由能斯特方程计算出来的平衡电位
B.原电池就是最原始的Cu-Zn电极组成的丹尼尔电池
C.电池的电动势为负值时就是原电池,否则就是电解池
D.可逆电极就是可以进行逆向电化学反应的电极
在298 K时,电池Hg(1) |Hg2Cl2(s) |HCl(a) |Cl2(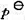 )|Pt(s)的电动势为1.092 V ,温度系数为 9.427×10-4V·K- 1.(1)写出有2个电子得失的电极反应和电池的净反应;(2)计算与该电池反应相应的
)|Pt(s)的电动势为1.092 V ,温度系数为 9.427×10-4V·K- 1.(1)写出有2个电子得失的电极反应和电池的净反应;(2)计算与该电池反应相应的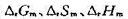 及可逆热效应QR。若只有1个电子得失,则这些值又等于多少?(3)计算在相同温度和压力下,与2个电子得失的电池净反应相同的热化学反应方程式的热效应。
及可逆热效应QR。若只有1个电子得失,则这些值又等于多少?(3)计算在相同温度和压力下,与2个电子得失的电池净反应相同的热化学反应方程式的热效应。
写出下列各电池的电池反应。应用表7.7.1(在教材中)的数据计算25℃时各电池的电动势及电池反应的摩尔吉布斯函数变,并指明各电池反应能否自发进行。
(1)Pt|H2(g,100kPa)|HCl[a(HCl)=1]|Cl2(g,100kPa)|Pt
(2)Zn|ZnCl2[a(ZnCl2)=0.5]|AgCl(S)|Ag
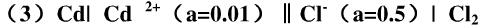
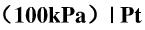
(1)计算下列反应的标准电极电位(其中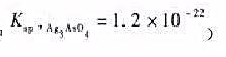 )
)
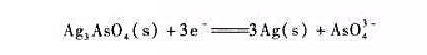
(2) 写出以Ag为指示电极,饱和甘汞电极(SCE)为参比电极,能用来测As063-活度的电池图解表达式。
(3)推导出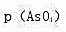 的表达式(不考虑液接电位)。
的表达式(不考虑液接电位)。
(4)在小题(2)所示的电池中,若测得电池的电动势为0.247V,计算饱和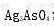 溶液中
溶液中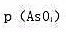 (温度为25℃)。
(温度为25℃)。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
