 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
钴的价电子构型是3d74s2,钴原子外层轨道中未成对电子数是()。A.1B.2C.3D.4
钴的价电子构型是3d74s2,钴原子外层轨道中未成对电子数是()。
A.1
B.2
C.3
D.4
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
钴的价电子构型是3d74s2,钴原子外层轨道中未成对电子数是()。
A.1
B.2
C.3
D.4
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“钴的价电子构型是3d74s2,钴原子外层轨道中未成对电子数是()。A.1B.2C.3D.4”相关的问题
更多“钴的价电子构型是3d74s2,钴原子外层轨道中未成对电子数是()。A.1B.2C.3D.4”相关的问题
| 下表为周期表的一部分,其中的编号代表对应的元素。
试填空。 (1)写出上表中元素I的基态原子的电子排布式和价层电子排布图: 。 元素C、D、E、F的第一电离能由大到小的顺序是 (用元素符号表示)。 (2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙。下列有关叙述不正确的有 。 A.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形 B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式 C.三种分子中键角由大到小的顺序是丙>乙>甲 D.甲、乙和丙分子均为由极性键构成的极性分子 (3)由元素J、C、E组成一种化学式为J(CE)5的配位化合物,该物质常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂。据此可判断: ①该化合物的晶体类型为 。 ②该化合物的晶体中存在的作用力有 。 A.离子键 B.极性键 C.非极性键 D.范德华力 E.氢键 F.配位键 ③根据共价键理论和等电子体理论分析,CE分子中σ键与π键的数目比为 。 (4)在测定A与F形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是 。 (5)某些不同族元素的性质也有一定的相似性,如表中元素G与元素B,原因是 。 |
选出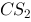 的中心原子价轨道的杂化类型和分子构型。(杂化类型和分子构型各选一个)
的中心原子价轨道的杂化类型和分子构型。(杂化类型和分子构型各选一个)
A、sp杂化
B、sp2杂化
C、sp3杂化
D、直线形
E、正四面体
F、平面三角形

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
