 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应Ag++e-====Ag和AgCl+e-====Ag+Cl-的标准电极电势分别为0.799V和0.2221V,计算AgCl的溶度积Ksp(AgCl)。
反应Ag++e-====Ag和AgCl+e-====Ag+Cl-的标准电极电势分别为0.799V和0.2221V,计算AgCl的溶度积Ksp(AgCl)。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应Ag++e-====Ag和AgCl+e-====Ag+Cl-的标准电极电势分别为0.799V和0.2221V,计算AgCl的溶度积Ksp(AgCl)。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“反应Ag++e-====Ag和AgCl+e-====Ag+Cl-的标准电极电势分别为0.799V和0.2221V,计算AgCl的溶度积Ksp(AgCl)。”相关的问题
更多“反应Ag++e-====Ag和AgCl+e-====Ag+Cl-的标准电极电势分别为0.799V和0.2221V,计算AgCl的溶度积Ksp(AgCl)。”相关的问题
用对消法测定由电极 Ag(s)│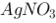 (aq) 与电极 Ag,AgCl(s)│KCl(aq) 组成的电池的电动势,下列 哪一项是不能采用的? ( )
(aq) 与电极 Ag,AgCl(s)│KCl(aq) 组成的电池的电动势,下列 哪一项是不能采用的? ( )
A、饱和KCl盐桥
B、标准电池
C、电位计
D、直流检流计
A、2.9×103kJ·mol-1
B、-114 kJ·mol-1
C、-110 kJ·mol-1
D、-13.9 kJ·mol-1
A、-0.15V
B、0.15V
C、0.10V
D、-0.10V
A、φ=φθ(O2/H2O)+0.0592pH
B、φ=φθ(O2/H2O)-0.0592pH
C、φ=φθ(O2/H2O)+0.0148pH
D、φ=φθ(O2/H2O)-0.0148pH
14.25℃时电极反应 Cu2+ + I - + e →CuI 和 Cu2+ + e → Cu+ 的标准电极电势分别为0.086V和0.153V,则CuI的溶度积Ksp为:
A、 1.2 × 10-12 ;
B、 6.2 × 10-6 ;
C、 4.8 × 10-7 ;
D、 2.9 × 10-15
称取5.00g钢样,经管式炉燃烧,生成的SO2被吸收后用碘标准液滴定,消耗3.00mL。碘标准溶液按下法计量配制:2.1400g KIO3与60gKI配成1L。计算钢样中硫含量。
称取2.200g KHC2O4·H2C2O4·2H2O配制于250mL容量瓶中,移取25.00mL,用NaOH滴定消耗24.00mL;移取25.00mL,于酸性介质中用KMnO4滴定消耗30.00mL,求此NaOH和KMnO4溶液的浓度。若用此KMnO4标准溶液测定样品中Fe含量,称取0.6000g样品消耗KMnO421.00mL,求算样品中Fe2O3的质量分数。
用0.02mol·dm-3KMnO4溶液滴定0.1mol·dm-3Fe2+溶液和用0.002mol·dm-3KMnO4溶液滴定0.01mol·dm-3Fe2+溶液两种情况下滴定突跃的大小将( )
A.相同 B.浓度大突跃越大
C.浓度小的滴定突跃大D.无法判断

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
