 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列弱酸的pKa:HAc=4.75,H2PO4ˉ=7.21HCO3ˉ=10.25NH4+=9.25,配制pH=5的溶液应选择的缓冲对
已知下列弱酸的pKa:HAc=4.75,H2PO4ˉ=7.21HCO3ˉ=10.25NH4+=9.25,配制pH=5的溶液应选择的缓冲对是()
AHAc-NaAc
BNaH2PO4-Na2HPO4
CNaHCO3--Na2CO3
DNH3-NH4Cl
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列弱酸的pKa:HAc=4.75,H2PO4ˉ=7.21HCO3ˉ=10.25NH4+=9.25,配制pH=5的溶液应选择的缓冲对是()
AHAc-NaAc
BNaH2PO4-Na2HPO4
CNaHCO3--Na2CO3
DNH3-NH4Cl
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“已知下列弱酸的pKa:HAc=4.75,H2PO4ˉ=7.21HCO3ˉ=10.25NH4+=9.25,配制pH=5的溶液应选择的缓冲对”相关的问题
更多“已知下列弱酸的pKa:HAc=4.75,H2PO4ˉ=7.21HCO3ˉ=10.25NH4+=9.25,配制pH=5的溶液应选择的缓冲对”相关的问题
A、HAc-NaAc
B、NaH2PO4-Na2HPO4
C、NaHCO3-Na2CO3
D、NH3-NH4Cl
已知: pKa2( ) = 7.21, pKa(HAc) = 4.75, pKb(
) = 7.21, pKa(HAc) = 4.75, pKb(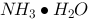 ) = 4.75, pKa2(
) = 4.75, pKa2(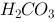 ) = 10.25。 欲配制pH≈9的缓冲溶液,应选择的缓冲对是 。
) = 10.25。 欲配制pH≈9的缓冲溶液,应选择的缓冲对是 。
A、 ~
~
B、HAc~NaAc
C、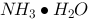 ~
~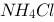
D、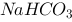 ~
~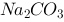
已知: pKa2( ) = 7.21, pKa(HAc) = 4.75, pKb(
) = 7.21, pKa(HAc) = 4.75, pKb(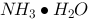 ) = 4.75, pKa2(
) = 4.75, pKa2(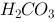 ) = 10.25。 欲配制pH≈9的缓冲溶液,应选择的缓冲对是 。
) = 10.25。 欲配制pH≈9的缓冲溶液,应选择的缓冲对是 。
A、 ~
~
B、HAc~NaAc
C、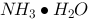 ~
~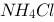
D、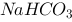 ~
~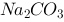
A.3.75
B.4.75
C.5.75
D.9.25
A.3.75
B.4.75
C.5.75
D.9.75
(A) 4.75
(B) 4.45
(C) 9.25
(D) 5.05
A.4.75
B.6.25
C.7.00
D.9.25
六、计算题(每小题10分,共40分) 1、计算下列混合溶液的pH值: 20mL 0.1 mol×L-1HAc与10mL 0.1 mol×L-1NaOH混合(已知:HAc PKa=4.75)。 2、在10mL 1.5×10-3mol/L MnSO4溶液中,加入5.0mL 0.15mol/L NH3·H2O溶液,能否生成Mn(OH)2沉淀? [已知:NH3·H2O的Kb =1.79×10-5;Mn(OH)2Ksp=2.06×10-13] 3、已知下列标准电极电势 Cu2++2e- =Cu Eq =0.337V Cu2++e-=Cu+ Eq =0.153V 计算反应 Cu + Cu2+ = 2Cu+的平衡常数。 4、计算下列混合溶液的pH值 20 ml 0.1 mol×L-1 HAc与10 ml 0.1 mol×L-1 NaOH混合(已知:HAc 的PKa= 4.75)

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
