 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
判断下列反应进行的方向,假设各离子的浓度都是1mol·dm-3:
判断下列反应进行的方向,假设各离子的浓度都是1mol·dm-3:
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
判断下列反应进行的方向,假设各离子的浓度都是1mol·dm-3:
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“判断下列反应进行的方向,假设各离子的浓度都是1mol·dm-3:”相关的问题
更多“判断下列反应进行的方向,假设各离子的浓度都是1mol·dm-3:”相关的问题
A. 液氨产品的净制系统与致冷回路不可独立
B. 液氨产品的净制系统与致冷回路即可合并又可分开
C. 液氨产品的净制系统与致冷回路不可合并
D. 以上答案都对
A、1006.61
B、-1006.61
C、675.05
D、-675.05
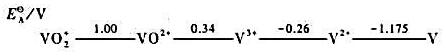
①钒如能溶解在稀酸中,将以何种氧化态存在?试写出化学反应方程式。
②写出V3+/V电对的Eθ。
③在这些不同氧化态物质间能否发生歧化反应?如能发生请写出化学反应方程式。
④将V放入含有V3+的溶液中,有无反应发生?若有请写出化学反应方程式。
(1)写出原电池符号、电池反应式;
(2)查标准电极电势表,求该原电池的标准电动势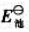 ;
;
(3)当电池反应进行到c(Cu2+)=1.0mol·dm-3时,试计算原电池的电动势E池。
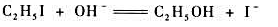
测得其288.83K时的速率常数k=5.03×10-5mol-1·dm-3·s-1,305.02K时的速率常数k=3.68×10-4mol-1·dm-3·s-1。试求该反应的活化能,并计算363.6IK时的速率常数。
B.0.8mol·L-1·s-1
C.0.2mol·L-1·s-1
D.0.6mol·L-1·s-1
(1)试结合图1.18.1所示的反应进程-势能图,定性判断该反应是吸热反应,还是放热反应,求算该反应的ΔtH;
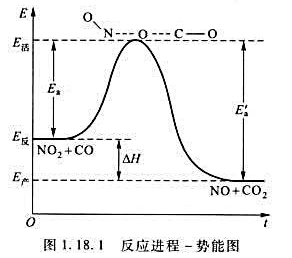
(2)若298K时的速率常数k=2.3×10-2s-1。试求373K时的速率常数;
(3)求算阿伦尼乌斯公式中的指前因子A。
25℃时,溶液中含有Fe3+、Fe2+,它们浓度都是0.05mol·dm-3,如果要求Fe(OH)3沉淀完全,而Fe2+不生成Fe(OH)2沉淀,试问溶液的pH应控制为多少?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
