 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
NaCl具有面心立方结构,其晶胞边长为0.564nm:
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“NaCl具有面心立方结构,其晶胞边长为0.564nm:”相关的问题
更多“NaCl具有面心立方结构,其晶胞边长为0.564nm:”相关的问题
Nacl具有面心立方结构,其晶胞边长为0.564 nm: (1)计算其密度; (2)某化合物AgX与NaCl结构相同,密度为6 477 kg.m-1,晶胞边长为0.5775 nm,确定X。
A.同属于面心立方点阵结构的晶体具有形状相同、大小不同的晶胞。
B.面心立方结构对应的实际晶体不只一种。
C.在面心立方结构的晶体中,原子或离子分布在立方体晶胞的角隅与6个外表面的中心。
D.同属于面心立方点阵结构的晶体,围绕其点阵中每个阵点的原子种类、数量及分布方式可能不同。
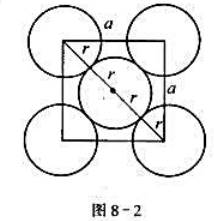
铜的密度为8.96g·cm-3,Cu属面心立方晶格,试求
晶胞边长及铜原子半径r(Cu原子量63.5)(见图8-2).
已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。
(I)写出通过晶胞中心的点对称元素。
(2)根据Na+和Cl-的离子半径值,了解在这结构中负离子是否接触?这种结构的稳定性如何?
(3)试计算NaCl晶体的密度D。
(4)将图C.17.1晶胞中顶角上的Na+和中心的Cl-除去,将Na+换成Nb2+,Cl-换得O2-即得NbO晶胞,试画出NbO的晶胞和其中原子簇的结构;已知晶跑参数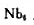 =421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
=421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
(5)将图C.17.1晶胞中面心和体心的原子除去,顶角上的Na+换成U6+,棱上的Cl-换成O2-,得UO3的晶体结构,立方晶胞参数a=415.6pm。试画出UO3晶胞的结构;写出通过晶胞中心点的点对称元素和点群;计算晶体的密度,计算U6+的离子半径(U的相对原子质量为238.0);画出由处在12条棱上的02-组成的立方八面体的图形;计算该多面体的自由孔径。
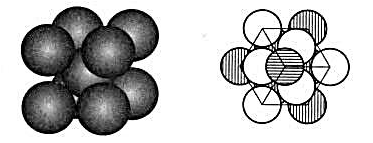
(1)试计算金属晶体中钾原子的空间占有率;
(2)试计算金属晶体中铂原子的空间占有率;
(3)已知铂的相对原子质量为195.08,若金属铂的立方晶胞的边长a=392.3pm,试计算每立方厘米金属铂的质量。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
