 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列配离子转化反应的平衡常数,并讨论之。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“计算下列配离子转化反应的平衡常数,并讨论之。”相关的问题
更多“计算下列配离子转化反应的平衡常数,并讨论之。”相关的问题
已知下列反应: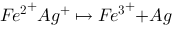 ,试计算: (1)反应的平衡常数
,试计算: (1)反应的平衡常数 ; (2)等体积混合1.0 mol/L的
; (2)等体积混合1.0 mol/L的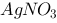 溶液和1.0 mol/L的
溶液和1.0 mol/L的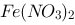 溶液,溶液中存在的各种离子的浓度。 已知:
溶液,溶液中存在的各种离子的浓度。 已知:
分别计算反应:
(1)
(2)
在25℃时的标准平衡常数,并讨论Fe(II)的还原性、在空气中的稳定性与介质酸度的关系。
己知:



A.热力学平衡常数与反应体系中各物质的活度有关,对一个反应体系来说,当其内物质的活度发生变化时该反应的热力学平衡常数也会发生变化;
B. 热力学平衡常数与反应体系中各物质的活度无关,但可以用反应达到平衡时体系内各物质的平衡活度进行计算;
C. 热力学平衡常数与温度无关,但可以用标准状态下反应的吉布斯自由能变进行计算;
D. 水的离子积KW实际上就是水离解反应的热力学平衡常数。
依据价键理论,说明下列配离子的中心原子外层轨道的杂化类型、配离子的几何构型,并计算磁矩。 (1)[Zn(NH3)4]2+(Z=30)。 (2)[FeF6]3—(Z=26)。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
