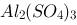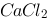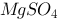题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下面四种电解质溶液,浓度均为0.01 mol·dm-3,现已按它们的摩尔电导率Lm值由大到小排了次序。请判定下面哪个是正确的?
A.NaCl > KCl > KOH > HCl
B.HCl > KOH > KCl > NaCl
C.HCl > NaCl > KCl > KOH
D.HCl > KOH > NaCl > KCl
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有5位网友选择 A,占比55.56%
- · 有3位网友选择 C,占比33.33%
- · 有1位网友选择 B,占比11.11%



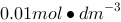 ,现已按它们的摩尔电导率Lm 值由大到小排了次序。请根据你已有的知识,判定下面哪个是正确的()。
,现已按它们的摩尔电导率Lm 值由大到小排了次序。请根据你已有的知识,判定下面哪个是正确的()。
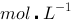 的下列四种溶液中,沸点最高的是 ()
的下列四种溶液中,沸点最高的是 ()