 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在锌、铜原电池中,电子流动的方法是()。
A.从锌流到铜
B.方向不断改变
C.从铜流到锌
D.电子不流动
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 B,占比40%
- · 有2位网友选择 C,占比20%
- · 有2位网友选择 A,占比20%
- · 有2位网友选择 D,占比20%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.从锌流到铜
B.方向不断改变
C.从铜流到锌
D.电子不流动
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“在锌、铜原电池中,电子流动的方法是()。”相关的问题
更多“在锌、铜原电池中,电子流动的方法是()。”相关的问题
A.铜锌组成原电池中电子是从锌经过导线流向铜
B.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌片放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
铜锌原电池工作图如图,下列叙述正确的是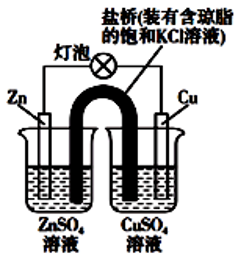
A、一段时间后,铜棒上有红色物质析出
B、正极反应为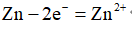
C、电子从负极流向正极,再经盐桥流回负极
D、盐桥中的 K+移向 ZnSO4溶液
A、Zn2+与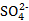 在溶液中的迁移速率不同,会产生电势差,两极之间形成液接电势
在溶液中的迁移速率不同,会产生电势差,两极之间形成液接电势
B、随着反应的进行,负极锌片周围的溶液带正电荷阻止锌失去电子变成Zn2+进入溶液,铜片周围的溶液带负电荷,阻止 Cu2+得到电子
C、在反应的过程中,锌片表面逐渐变得光滑,难以吸附电子
D、锌表面形成 “铜锌原子电池”
A.将反应2Fe3++Fe===3Fe2+设计为原电池,则可用Zn为负极,Fe为正极,FeCl3为电解质
B.铜片和铝片用导线连接后插入浓硝酸中,铜作负极
C.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
D.铝片和镁片用导线连接后插入NaOH溶液中,Mg较活泼作负极
铜锌原电池工作时(CuSO4/Cu,ZnSO4/Zn),下列叙述正确的是()
A.实验过程中取出盐桥,原电池仍继续工作
B.将Zn片浸入CuSO4溶液中,发生的化学反应与该原电池反应相同
C.在外电路中,电子从正极流向负极
D.盐桥中的K+移向ZnSO4溶液
A.能将化学能转化为电能
B.电子从Cu经导线流向Zn
C.溶液中H+、SO42-分别向铜、锌电极移动
D.该装置中发生的总反应为:Zn+2H+=Zn2++H2↑
某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中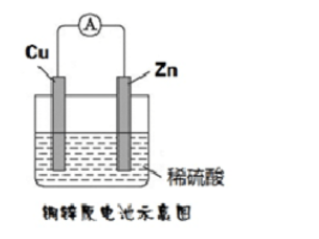 (1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(2)若反应过程中有0.2mol电子发生转移,则生成的气体在标准状况下的体积为()。
(3)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是()(填序号)。
A.无水乙醇
B.醋酸溶液
C.CuSo4溶液
D.苯
(4)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是()(填字母代号)。
A.NaOH+HCl=NaCl+H2O
B.2H2+O2=2H2O
C.Fe+2FeCl3=3FeCl2
D.2H20=2H2↑+2O2↑
A.锌是负极,铜是正极
B.标准状态下,铜电极电势高于锌电极电势
C.在铜电极溶液中滴加氨水,原电池电动势将减小
D.在锌电极溶液中滴加氨水,锌电极电势会增大

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
