 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在同一温度下用化学方程式N [图](g)+3H [图](g) ?2N...
在同一温度下用化学方程式N+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/73302ca-chaoxing2016-539076.png) (g)+3H
(g)+3H+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/73302ca-chaoxing2016-539076.png) (g) ⇌2NH
(g) ⇌2NH+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/e2dcbb2-chaoxing2016-539184.png) (g)或用 1/2N
(g)或用 1/2N+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/73302ca-chaoxing2016-539076.png) (g)+3/2H
(g)+3/2H+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/73302ca-chaoxing2016-539076.png) (g) ⇌NH
(g) ⇌NH+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/e2dcbb2-chaoxing2016-539184.png) (g) ,前者的平衡常数是后者的两倍。()
(g) ,前者的平衡常数是后者的两倍。()
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在同一温度下用化学方程式N+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/73302ca-chaoxing2016-539076.png) (g)+3H
(g)+3H+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/73302ca-chaoxing2016-539076.png) (g) ⇌2NH
(g) ⇌2NH+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/e2dcbb2-chaoxing2016-539184.png) (g)或用 1/2N
(g)或用 1/2N+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/73302ca-chaoxing2016-539076.png) (g)+3/2H
(g)+3/2H+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/73302ca-chaoxing2016-539076.png) (g) ⇌NH
(g) ⇌NH+3H [图](g) ?2N...在同一温度下用化学方程](http://static.jiandati.com/e2dcbb2-chaoxing2016-539184.png) (g) ,前者的平衡常数是后者的两倍。()
(g) ,前者的平衡常数是后者的两倍。()
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 更多“在同一温度下用化学方程式N [图](g)+3H [图](g) ?2N...”相关的问题
更多“在同一温度下用化学方程式N [图](g)+3H [图](g) ?2N...”相关的问题
反应NO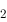 (g) +NO (g) ⇌N
(g) +NO (g) ⇌N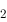 O
O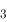 (g) 的
(g) 的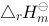 = –40.5kJ·mol
= –40.5kJ·mol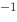 ,反应达平衡时,下列因素中可使平衡逆向移动的是( )
,反应达平衡时,下列因素中可使平衡逆向移动的是( )
A、T一定,V一定,压入氖气
B、T一定,V变小
C、V一定,p一定,T升高
D、以上都不对
某气体反应 A(g) +B(g) = 2C(g) 的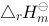 (298K) = 100 kJ·mol
(298K) = 100 kJ·mol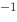 , 对此反应的逆反应来说,下列说法中正确的是( )
, 对此反应的逆反应来说,下列说法中正确的是( )
A、升高温度,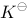 值将减小
值将减小
B、升高温度,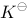 值将增大
值将增大
C、增大压强平衡将向正反应方向移动
D、增加C 的浓度,对平衡无影响
当反应A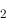 +B
+B →2AB的速率方程为v=kc(A
→2AB的速率方程为v=kc(A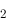 )c(B
)c(B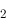 )时,则此反应( )。
)时,则此反应( )。
A、一定是基元反应
B、一定是非基元反应
C、不能肯定是否为基元反应
D、反应为一级反应
A、活化能大的反应其反应速率慢
B、加入正催化剂可降低反应的活化能
C、不同反应有不同的活化能
D、升高温度,活化能小的反应其反应速率增加的倍数反而比活化能大的反应其反应速率增加的倍数更多
反应C(s)+O (g) →CO
(g) →CO (g) 为放热反应, 欲增加正反应速率,下列措施中无用的是( )。
(g) 为放热反应, 欲增加正反应速率,下列措施中无用的是( )。
A、增加氧的分压
B、减少CO 的分压
的分压
C、使用催化剂
D、升高温度

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
