 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
应用附录中有关物资的热化学数据,计算25°C时反应的标准摩尔反应始,要求: (1)应用25°C的
应用附录中有关物资的热化学数据,计算25°C时反应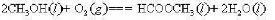 的标准摩尔反应始,要求:
的标准摩尔反应始,要求: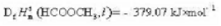
(1)应用25°C的标准摩尔生成焓数据:
(2)应用25°C的标准摩尔燃烧焓数据。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
应用附录中有关物资的热化学数据,计算25°C时反应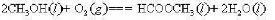 的标准摩尔反应始,要求:
的标准摩尔反应始,要求: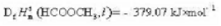
(1)应用25°C的标准摩尔生成焓数据:
(2)应用25°C的标准摩尔燃烧焓数据。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“应用附录中有关物资的热化学数据,计算25°C时反应的标准摩尔反应始,要求: (1)应用25°C的”相关的问题
更多“应用附录中有关物资的热化学数据,计算25°C时反应的标准摩尔反应始,要求: (1)应用25°C的”相关的问题
化学反应如下:
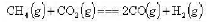
(1)利用附录中各物质的数据,求上述反应在25°C时的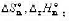
(2)利用附录中各物质的数据,计算上述反应在25°C时的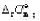
(3)25°C若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的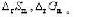
将下列反应设计成原电池,并应用教材中表7.7.1的数据计算25℃时电池反应的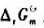 及
及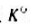 .
.
(1)2Ag++H2(g)=2Ag+2H+
(2)Cd+Cu2+=Cd2++Cu
(3)Sn2++Pb2+=Sn4++Pb
(4)2Cu+=Cu+Cu2+
已知化学反应式CH4(g)+CO2(g)===2CO(g)+2H2(g):
(1)利用附录(在教材中)中各物质的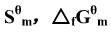 ,数据,求上述反应在25℃时的
,数据,求上述反应在25℃时的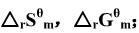
;(2)利用附录(在教材中)中各物质的△rGm数据,求上述反应在25℃时的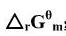 ;
;
(3)25℃时,若始态CH4(g)和CO2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的△rSm和△rGm。
(1)应用表7.7.1(在教材中)的数据计算反应Fe2++Ag+===Fe3++Ag在25℃时的平衡常数KΘ。(2)将适量的银粉加到浓度为0.05mol·dm-3的Fe(NO3)3溶液中,计算平衡时Ag+的浓度(假设各离子的活度因子均等于1)。
应用德拜-休克尔公式计算25℃时下列各溶液中的γ±:
(1)0.005mol·kg-1NaBr;(2)0.001mol·kg-1ZnSO4。
A.引言
B.ISO 9000质量管理体系过程方法
C.ISO 9001:2000在工程咨询服务中的应用
D.ISO 9001:2000要求用于工程咨询业的解释
E.附录
试查阅附录3的数据计算下列反应的△rHΘm(298.15 K)。 (1)4NH3(g)+3O2(g) 2N2(g)+6H2O(1) (2)C2H2(g)+H2(g)=C2H4(g) (3)NH3(g)+稀盐酸 (4)Fe(s)+CuSO4(aq) 分析本题主要考查利用标准热力学数值ArHΘm求反应焓变△rHΘm查△fHΘm数据时要注意物质的状态,对于水溶液中的反应可抓住其实质——离子反应进行计算。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
