 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电解液的pH为4.30,在H2逸出之前,为使Zn2+浓度降至1.0×10-6mol·L-1所必需的氢的过电位是多少?
电解液的pH为4.30,在H2逸出之前,为使Zn2+浓度降至1.0×10-6mol·L-1所必需的氢的过电位是多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电解液的pH为4.30,在H2逸出之前,为使Zn2+浓度降至1.0×10-6mol·L-1所必需的氢的过电位是多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“电解液的pH为4.30,在H2逸出之前,为使Zn2+浓度降至1.0×10-6mol·L-1所必需的氢的过电位是多少?”相关的问题
更多“电解液的pH为4.30,在H2逸出之前,为使Zn2+浓度降至1.0×10-6mol·L-1所必需的氢的过电位是多少?”相关的问题
A. 0.0500mol/L
B. O.0250mol/L
C. O.0125mol/L
D. O.0025mol/L
A、0.10mol·L-1Na2HPO4>0.10mol·L-1H3PO4
B、0.10mol·L-1Na2HPO4>0.10mol·L-1NaH2PO4
C、0.10mol·L-1NaH2PO4>0.10mol·L-1H3PO4
D、0.10mol·L-1KH2PO4>0.10mol·L-1Na2HPO4
在pH=10.0的氨性溶液中,已计算出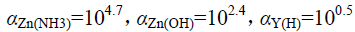 ,在此条件下,
,在此条件下,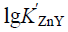 为( ) (已知
为( ) (已知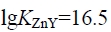 )
)
A、8.9
B、11.8
C、14.3
D、11.3
一溶液含0.1mol·L-1Cd2+和1mol·L-1Zn2+,用饱和甘汞电极作参比电极(0.244V)电解此溶液,当cH+=1mol·L-1时:
(1)欲使Zn2+不析出,阴极上可能施加的负电压是多少?
(2)在此电压时溶液中还残留多少Cd2+?
(3)为使99.9%Cd2+沉积所需的负电压至少是多少?
电解镉时,为使Cd2+浓度降至1.0×10-6mol·L-1而不逸出H2,试从理论上计算溶液的pH必须等于多少。
对于电解池Pt|Ag+(0.2mol·L-1)||H+(0.2mol·L-1)|Pt:

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
