 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,1.0L0.1mol·L-1的NH3·H2O溶液中加入NH4Cl晶体(设溶液体积不变),则使______。
A.NH3·H2O的解离常数增大
B.NH3·H2O解离度增大
C.溶液的pH值增大
D.溶液的pH值降低
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 B,占比40%
- · 有3位网友选择 A,占比30%
- · 有2位网友选择 D,占比20%
- · 有1位网友选择 C,占比10%



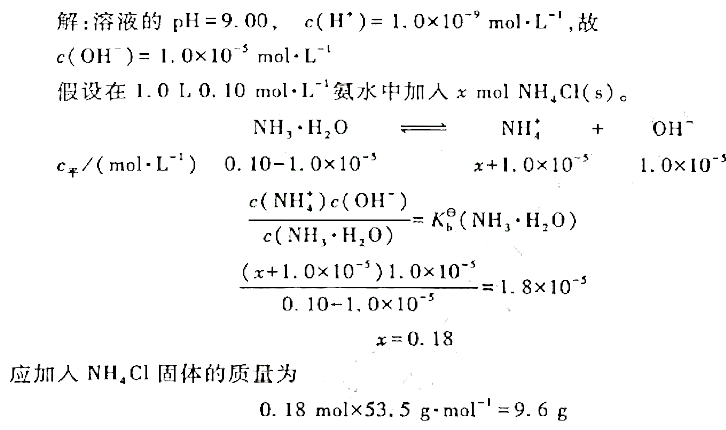
![25℃时,计算25℃时0.010mol·L-1[Ag(S2O2)2]3-溶液中S2O3225℃时,计](https://img2.soutiyun.com/ask/2020-10-13/971478586672093.png) 计算25℃时0.010mol·L-1[Ag(S2O2)2]3-溶液中S2O32-[Ag(S2O3)2]3-和Ag+的平衡浓度。
计算25℃时0.010mol·L-1[Ag(S2O2)2]3-溶液中S2O32-[Ag(S2O3)2]3-和Ag+的平衡浓度。




























