 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友18***590
发布时间:2022-06-03
[主观题]
试利用标准电极电势的数据(表5.5)计算298K时反应的平衡常数.
试利用标准电极电势的数据(表5.5)计算298K时反应的平衡常数.
试利用标准电极电势的数据(表5.5)计算298K时反应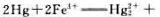
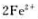 的平衡常数
的平衡常数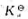 .
.
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
查看官方参考答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试利用标准电极电势的数据(表5.5)计算298K时反应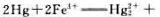
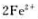 的平衡常数
的平衡常数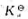 .
.
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“试利用标准电极电势的数据(表5.5)计算298K时反应的平衡常数.”相关的问题
更多“试利用标准电极电势的数据(表5.5)计算298K时反应的平衡常数.”相关的问题
A.标准状态下稳定的单质的电极电势为0
B.绝对0度时稳定单质的电极电势为0
C.标准氢电极的电极电势为0
D.298 K时的稳定单质的电极电势为0
298K时,已知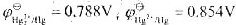 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
已知下列标准电极电势:EΘ(Cu2+/Cu)=0.340V,EΘ(Cu2+/Cu+)=0.159V,Ksp(CuCl)=1.72×10-7,试计算下列反应的标准平衡常数: (1)Cu2++Cu=2Cu+; (2)Cu2++Cu+2Cl-=2CuCl(s)。
已知25°C时AgBr的溶度积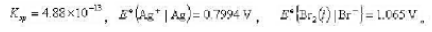 试计算25°C时
试计算25°C时
(1)银-溴化银电极的标准电极电势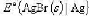 ;
;
(2)AgBr(s)的标准生成吉布斯函数。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
