 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
钢在热处理时易被氧化,已知反应Fe(s)+1/2O2(g)=FeO(s) 该反应的△rGΘm(773K)=-16.97kJmol-1,欲使
钢在热处理时易被氧化,已知反应Fe(s)+1/2O2(g)=FeO(s) 该反应的△rGΘm(773K)=-16.97kJmol-1,欲使钢件在500℃加热进行热处理时不被氧化,应如何控制炉内O2的分压。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
钢在热处理时易被氧化,已知反应Fe(s)+1/2O2(g)=FeO(s) 该反应的△rGΘm(773K)=-16.97kJmol-1,欲使钢件在500℃加热进行热处理时不被氧化,应如何控制炉内O2的分压。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“钢在热处理时易被氧化,已知反应Fe(s)+1/2O2(g)=FeO(s) 该反应的△rGΘm(773K)=-16.97kJmol-1,欲使”相关的问题
更多“钢在热处理时易被氧化,已知反应Fe(s)+1/2O2(g)=FeO(s) 该反应的△rGΘm(773K)=-16.97kJmol-1,欲使”相关的问题
钢铁进行热处理时,应控制处理气氛,防止铁的氧化。已知850℃=时,反应为
Fe(s)+CO2(g)=FeO(s)+CO(g) KΘ=2.4
(1)若系统中只有CO2和CO两种气体,二者比例为多少可防止Fe(s)的氧化?
(2)若系统中加入ψ(N2)=0.40的惰性气体N2,则CO与CO2的比例为多少可防止Fe(s)的氧化?
判断下列反应在标准态时进行的方向,如能正向进行,试计算反应进行的程度。已知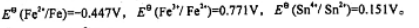
(1)Fe(s)+2Fe3+(aq)=3Fe2+(aq)
(2)Sn4+(aq)+2Fe2+(aq)=Sn2+(aq)+2Fe3+(aq)
分析:首先根据反应方程确定电池的正负极,即发生氧化反应的电对为负极,发生还原反应的为正极,然后根据正负极的电极电势的大小(若不是标准状态,则要根据能斯特方程计算出来)即电池的电动势的正负来判断反应的方向,并利用Kθ和标准电极电势的关系计算出反应进行的程度。
已知Fe3+(三价铁离子)与水反应生成的主要配合物及平衡常数如下: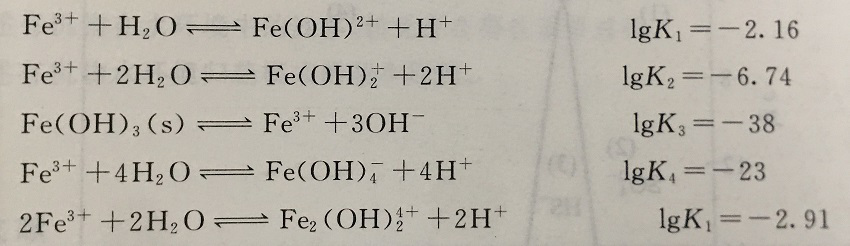 请计算Fe(OH)3(s)溶于水后各种离子的p[某种离子]与pH的关系。(以上方程式均不涉及氧化还原反应)(注意:最后一个方程式中lgK1改为lgK5)
请计算Fe(OH)3(s)溶于水后各种离子的p[某种离子]与pH的关系。(以上方程式均不涉及氧化还原反应)(注意:最后一个方程式中lgK1改为lgK5)
配制FeSO4溶液时,一般会加少量金属Fe来防止Fe2+被氧化,其原因是()。
A.加入金属Fe后,氧气不氧化Fe2+了
B.Fe3+可与Fe反应生成Fe2+
C.金属Fe可与溶液中的氢离子反应生成Fe2+
D.金属Fe在溶液中起导电作用
通过计算说明在298.15K、标准压力下,用C还原Fe2O3生成Fe和CO2在热力学上是否可能?若要反应自发进行,温度最低为多少?已知298.15K时相关热力学数据如下:
3C(石墨)+2Fe2O3(s)====4Fe(s)+3CO2(g)

1000K 时反应 Fe(s) + CO2(g) = FeO(s) + CO(g) 的 Kө=1.84,当 气相中CO2 和 CO的摩尔数之比为 65∶35时,则() AFe 不会被氧化
BFe 将被氧化
C正好达化学平衡
D难于判断其进行方向

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
