 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友zzp0706
发布时间:2022-01-07
[主观题]
将压力为 33.3 kPa的 H2 3.0 dm3和 26.0 kPa的He 1.0 dm3在 2.0 dm3的容器中混合均匀, 假定温度不变, 则p(H2)= ______ kPa.
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 更多“将压力为 33.3 kPa的 H2 3.0 dm3和 26.0 kPa的He 1.0 dm3在 2.0 dm3的容器中混合均匀, 假定温度不变, 则p(H2)= ______ kPa.”相关的问题
更多“将压力为 33.3 kPa的 H2 3.0 dm3和 26.0 kPa的He 1.0 dm3在 2.0 dm3的容器中混合均匀, 假定温度不变, 则p(H2)= ______ kPa.”相关的问题
(1)保持容器内温度恒定抽去隔板,计算气体混合后的压力;
(2)分别计算混合气体中H2和 N2的分压;
(3)分别计算混合气体中H2和N2的分体积.
(1)爆炸反应后100C时H2的分压;
(2)反应前O2的体积;
(3)反应后85℃时气体的体积。
A. 肺炎
B. 胸膜炎
C. 慢性阻塞性肺疾病,肺心病
D. 肺癌
E. 支气管扩张
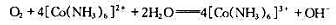
的平衡常数K.
(2)现将空气( =20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
=20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
[Co(NH3)6]3+,2.0mol·dm-3NH2+及2.0mol·dm-3NH3·H2O的混合溶液中,能否发生上述反应?
A、1.57 mol
B、1 mol
C、2 mol
D、3.14 mol
萘燃烧的化学反应方程式为: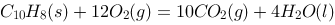 (l),则298 K时,
(l),则298 K时,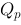 和
和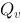 的差值为( )
的差值为( )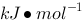 。
。
A、- 4.95
B、4.95
C、- 2.48
D、2.48

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
