 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在1~18号元素中,电子总数是最外层电子数二倍的元素是__________,最外层电子数是次外层
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“在1~18号元素中,电子总数是最外层电子数二倍的元素是__________,最外层电子数是次外层”相关的问题
更多“在1~18号元素中,电子总数是最外层电子数二倍的元素是__________,最外层电子数是次外层”相关的问题
A.第二周期第IA族
B.第三周期第ⅣA族
C.第二周期第VA族
D.第三周期第VA族
A,B,C,D,E和F元素为6种短周期元素,A,B和C3种元素基态原子的次外层电子排布式都是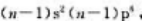 D,E和F3种元素的原子序数分别等于A.B和C元素基态原子的最外层电子数;在标准状况下1L气态C单质的质量3.17g;A元素与C元素能形成离子化合物AC,A离子比C离子少1个电子层,E原子的最外层p能级的电子数等于前一个电子层的电子总数。回答下列问题:
D,E和F3种元素的原子序数分别等于A.B和C元素基态原子的最外层电子数;在标准状况下1L气态C单质的质量3.17g;A元素与C元素能形成离子化合物AC,A离子比C离子少1个电子层,E原子的最外层p能级的电子数等于前一个电子层的电子总数。回答下列问题:
(1)上述元素基态原子中,含有2个未成对电子的元素是()。
(2)A元素与D元素能形成离子化合物AD,则离子化合物AD的化学式是()。
(3)写出C元素的基态原子的电子排布式()。
(4)写出F元素的基态原子的价电子的排布式()。
X、Y、Z、W是元素周期表中前30号元素,且原子序数依次增大。其相关信息如下表:
(1)W位于元素周期表第____周期第____族,其基态原子最外层有____个电子。 (2)X的第一电离能比Y的____(填“大”或“小”),1mol X22-中含有的 (3)X和Y的气态氢化物中,较稳定的是____(写化学式),Y的同族元素(包括Y)的最简单氢化物中沸点最低的是____。 (4)写出KZY3与HZ浓溶液反应制取Z2的化学方程式,并标出电子转移的方向和数目____。 (5)已知:X(s)+Y2(g)=XY2(g) ΔH1= -393.5 kJ?mol-1 XY(g) +1/2Y2(g)=XY2(g) ΔH2= -282.9 kJ?mol-1 则X(s)与Y2(g)反应生成XY(g)的热化学反应方程式为____。 |
A.3p能级有一个空轨道的基态原子和核外电子的排布为1s 2 2s 2 2p 6 3s 2 3p 2 的原子
B.2p能级无空轨道,且有一个未成对电子基态原子和原子的最外层电子排布为2s 2 2p 5 的原子
C.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s 2 4p 5 的原子
D.M层全充满而N层为4s 2 的原子和核外电子排布为1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
